
Na+ 、F- 、Ne可以归为一类,可与它们同为等电子体(即核外电子总数相等的微粒)的粒子组是 ( )
A.H2O 、Ar B.K+ 、H3O+ C.NH3 、NH4+ D. OH- 、 O22-
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | |||||||||||||||||
| D | F | ||||||||||||||||
| G | Q | M | R | ||||||||||||||
| N | |||||||||||||||||
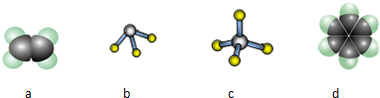
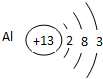
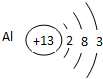
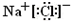
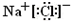
查看答案和解析>>
科目:高中化学 来源: 题型:
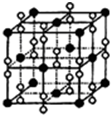
| 4×72 |
| a3×NA |
| 4×72 |
| a3×NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:NH3>PH3>SiH4 | B、微粒半径:K+>Na+>Mg2+>Al3+ | C、氢键的作用能F-H…F>O-H…O>N-H…N | D、电负性:F>N>O>C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com