
【题目】CH4是一种重要的化工原料,工业上以CH4为原料制备H2的原理为CH4(g)+H2O(g)![]() CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta。下列说法正确的是( )
CO(g)+3H2(g)。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1molCH4(g)和1.1molH2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a的体积为10L,温度为Ta。下列说法正确的是( )

A.a、b两容器的温度不可能相同
B.在达到平衡前,容器a的压强保持不变
C.该反应在Ta温度下的平衡常数为2700(mol·L-1)2
D.容器a中CH4从反应开始到恰好平衡时的平均反应速率为0.25mol·L-1·min-1
【答案】A
【解析】
通过图像可知,平衡时a装置中的CO的物质的量比b装置中的CO的物质的量大,反应时间短,说明a中化学反应速率较大。在两容器中起始投料相同的条件下,加快化学反应速率的措施有升高温度和增大压强两种方法。若a中压强较大,则相对于b来说,平衡逆向移动,CO的物质的量会小于b,故不可能;若a中温度高于b,相对于b来说,平衡正向移动,CO的浓度增大,则该反应的△H>0,有可能。
A.通过图像可知,平衡时a装置中的CO的物质的量比b装置中的CO的物质的量大,反应时间短,说明a中化学反应速率较大。在两容器中起始投料相同的条件下,加快化学反应速率的措施有升高温度和增大压强两种方法。若a中压强较大,则相对于b来说,平衡逆向移动,CO的物质的量会小于b,故不可能;若a中温度高于b,相对于b来说,平衡正向移动,CO的浓度增大,则该反应的△H>0,有可能。综上所述,a、b两容器中的温度不可能相同,A正确;
B.a为恒温恒容装置,压强与物质的量成正比,反应前反应物减少,生成物增多,总物质的量增大,压强增大,B错误;
C. CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
初始量 1.1 1.1 0 0
反应量 1 1 1 3
平衡量 0.1 0.1 1 3 K=0.1×0.33/(0.01×0.01)=27,C错误;
D. 容器a中CH4从反应开始到恰好平衡时的平均反应速率=1/(10×4)=0.025 mol·L-1·min-1,D错误;
答案为A


科目:高中化学 来源: 题型:
【题目】下列化学方程式书写错误的是
A.乙醇催化氧化制取乙醛:2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
B.乙烯使溴的四氯化碳溶液褪色:CH2=CH2+Br2→CH2Br—CH2Br
C.CH4和Cl2混合后光照:CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
D.乙酸和乙醇发生反应生成乙酸乙酯:CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于蔗糖属于非还原型糖,而其水解产物具有还原性的实验方案的说法中,正确的是
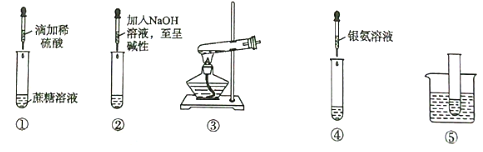
A. 验证蔗糖属于非还原型糖的操作顺序:④③
B. 验证蔗糖属于非还原型糖的操作顺序:③⑤
C. 验证蔗糖水解产物具有还原性的操作顺序:①④⑤
D. 验证蔗糖水解产物具有还原性的操作顺序:①⑤②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为2 L的密闭容器内, 某一反应中气体M和气体N的物质的量随反应时间变化的曲线如图所示, 请根据图示回答下列问题。
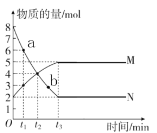
(1)写出该反应的化学方程式:____________。
(2)t1~t3时间段,以M的浓度变化表示的平均反应速率为________(用含t1、t3的式子表示)。
(3)比较a点与b点反应速率大小,Va___Vb(填“>”“=” 或 “< ”)。
(4)如图所示的三个时刻中,___________(填t1、t2或t3)时刻处于平衡状态。
(5)下列叙述中,能说明该反应达到平衡状态的是________。
A.容器内M与N的物质的量相等
B.容器内M与N的浓度不随时间变化
C.单位时间内每消耗1 mol N,同时生成0.5 mol M
D.容器内压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为一常见的坐标曲线图。该图能够表示的生物学含义是

A. 人红细胞中K+吸收量随O2浓度变化的情况
B. 细胞代谢中反应速率随底物浓度变化的情况
C. 某植物光合作用速率随光照强度变化的情况
D. 萌发的种子中自由水含量随时间变化的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z原子半径的顺序为![]() ,基态X原子p能级上的电子数是Y原子质子数的3倍,它们可以形成离子化合物
,基态X原子p能级上的电子数是Y原子质子数的3倍,它们可以形成离子化合物![]() ,其中阳离子
,其中阳离子![]() (已知
(已知![]() 水合物的
水合物的![]() 为
为![]() 、
、![]() 为
为![]() )的结构如图所示。下列叙述错误的是( )
)的结构如图所示。下列叙述错误的是( )
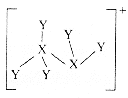
A.![]() 的阴、阳离子均含有18个电子
的阴、阳离子均含有18个电子
B.常温下,![]() 的水溶液呈碱性
的水溶液呈碱性
C.三种元素中Y的电负性最小
D.简单气态氢化物的还原性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用平衡移动原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深
C. 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 石灰岩受地下水长期溶蚀形成溶洞
石灰岩受地下水长期溶蚀形成溶洞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,利用煤化工中生产的CO、CO2和H2可制取甲醇等有机物,发生的反应有:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-99kJmol-1
CH3OH(g) △H1=-99kJmol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
相关物质的化学键键能数据如下:CH3OH结构式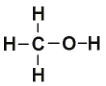
化学键 | C=O(CO2) | H—H | C—O | H—O | C—H |
E/(kJ·mol-1) | 803 | 436 | 343 | 465 | 413 |
(1)该反应△H2=____________。
(2)关于反应①下列说法,正确的是____________。
A.该反应在任何温度下都能自发进行
B.升高温度,正反应速率增大,逆反应速率减小
C.使用催化剂,不能提高CO的转化率
D.增大压强,该反应的化学平衡常数不变
(3)在某温度下,将1.0moCO与2.0molH2充入2L的空钢瓶中,发生反应①,在第5min时达到化学平衡状态,此时甲醇的物质的量分数为0.1。在第10min、20min时分别改变反应条件,甲醇的浓度在不同条件下的变化状况如图所示:

①从反应开始到5min时,生成甲醇的平均速率为____________。
②H2的平衡转化率α=____________%,化学平衡常数K=____________。
③1min时,υ正____________υ逆(填“大于”“小于”或“等于”)
④1mim时υ正____________4min时υ逆(填“大于”“小于”或“等于”)
⑤比较甲醇在7~8min、12~13min和25~27min时平均反应速率[平均反应速率分别以υ(7~8)、υ(12~13)、υ(25~27)表示的大小____________。
⑥若将钢瓶换成同容积的绝热容器,重复上述试验,平衡时甲醇的物质的量分数____________0.1(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
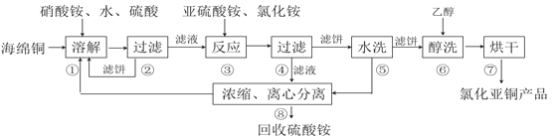
回答下列问题:
(1)步骤①中得到的氧化产物是_________,溶解温度应控制在60~70度,原因是__________。
(2)写出步骤③中主要反应的离子方程式___________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是______________________________。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有__________(填字母)
A.分馏塔 | B.离心机 | C.反应釜 | D.框式压滤机 |
(6)准确称取所制备的氯化亚铜样品m g,将其置于若两的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com