


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
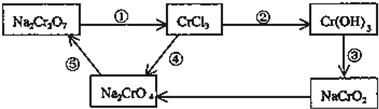
查看答案和解析>>
科目:高中化学 来源: 题型:
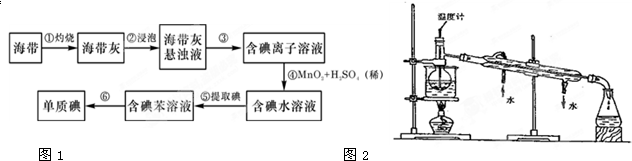
查看答案和解析>>
科目:高中化学 来源: 题型:
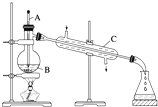 选择下列实验方法分离物质,将分离方法的序号填在横线上.
选择下列实验方法分离物质,将分离方法的序号填在横线上.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大力开发丰富的煤炭资源,减少对石油的依赖 |
| B、在西部和沿海地区兴建风力发电站,解决能源问题 |
| C、世博会很多场馆的外壳使用非晶硅薄膜,以充分利用太阳能,体现低碳经济 |
| D、世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com