
分析 (1)根据n=$\frac{m}{M}$计算相同质量的SO2气体和SO3气体的物质的量之比,结合分子中O原子数目计算二者含有氧原子数目之比,同温同压下体积之比等于物质的量之比、密度之比等于摩尔质量之比;
(2)令混合气体的质量为100g,根据氧元素的质量分数计算S元素质量分数,进而计算S元素质量,再计算SO2的质量、氧气的质量,根据n=$\frac{m}{M}$计算二者物质的量,根据平均相对分子质量=$\frac{m总}{n总}$计算平均相对分子质量,相同条件下,不同物质的密度之比等于其摩尔质量之比;
(3)根据物质的构成特点判断,由化学式可知,Al2(SO4)3中n(Al3+):n(SO42-)=2:3,以此解答该题;
(4)根据质量守恒计算C的质量,再根据M=$\frac{m}{n}$计算C的摩尔质量;
(5)由化学式可知3n(MCl3)=n(Cl-),据此计算n(MCl3),再根据M=$\frac{m}{n}$计算MCl3的摩尔质量,进而计算M的相对原子质量.
解答 解:(1)SO2气体和SO3气体的摩尔质量分别为64g/mol、80g/mol,则相同质量的SO2气体和SO3气体的物质的量之比=$\frac{1}{64}$:$\frac{1}{80}$=5:4,故二者分子数之比是5:4,含有O原子数目之比=5×2:4×3=5:6,同温同压下体积之比等于物质的量之比,故二者体积之比=5:4,同温同压下密度之比等于摩尔质量之比,故二者密度之比=64g/mol:80g/mol=4:5,
故答案为:5:4;5:6;5:4;4:5;
(2)SO2与O2的混合气体中,氧元素的质量分数为70%,则S元素的质量分数=1-70%=30%,令混合气体的质量为100g,则S元素质量=100g×30%=30g,故SO2的质量=30g÷$\frac{\frac{30}{32}}{64}$=60g.则氧气的质量=100g-60g=40g,则SO2的物质的量=$\frac{60g}{64g/mol}$=$\frac{15}{16}$mol,O2的物质的量=$\frac{40g}{32g/mol}$=$\frac{20}{16}$mol,则SO2与O2的物质的量之比为$\frac{15}{16}$mol:$\frac{20}{16}$mol=3:4,二者平均相对分子质量=$\frac{100}{\frac{15}{16}+\frac{20}{16}}$=45.71,相同条件下,气体的摩尔质量之比等于其密度之比,所以混合气体的密度是同温同压下氧气密度的倍数=$\frac{45.71}{32}$=$\frac{10}{7}$,
故答案为:3:4;$\frac{10}{7}$.
(3)Al2(SO4)3中n(Al3+):n(SO42-)=2:3,n(Al3+)=0.4mol,则n(SO42-)=0.6mol,故答案为:0.6mol;
(4)根据质量守恒定律知,C的质量=(16+20-31.76)g=4.24g,C的摩尔质量=$\frac{4.24g}{0.04mol}$=106g/mol,故答案为:106g/mol;
(5)金属氯化物MCl3 13.35g,含有Cl- 0.3mol,则n(MCl3)=$\frac{0.3mol}{3}$=0.1mol,MCl3的摩尔质量=$\frac{13.35g}{0.1mol}$=133.5g/mol,故M的相对原子质量=133.5-35.5×3=27,
故答案为:133.5g/mol;27.
点评 本题考查有关物质的量的计算,比较基础,侧重对基础知识的巩固,注意理解摩尔质量与质量、物质的量的关系,掌握相对分子质量的计算常用方法.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 两种元素组成的分子中所含化学键一定都是极性键 | |
| B. | 金属晶体的熔点一定比分子晶体的高 | |
| C. | 某晶体中含有阳离子,则一定也含有阴离子 | |
| D. | 含有阴离子的化合物一定含有阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 家用电器起火 常用液态CO2灭火 一般不用液态四氯化碳 | |
| B. | 将一氧化碳中毒者移到通风处抢救 | |
| C. | 眼睛里不慎溅进了药液 应立即用水冲洗 边洗边眨眼睛 不可用手揉眼睛 | |
| D. | 实验后 剩余的药品不能随便丢弃 或浪费 应放回原瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
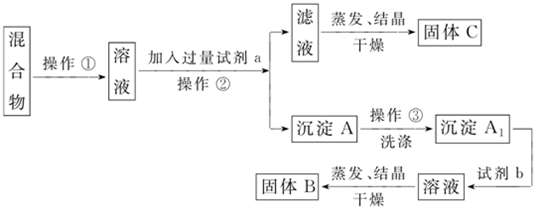
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温度、同体积的N2和O2 | B. | 同压强、同体积的H2和CH4 | ||
| C. | 同质量、不同密度的N2和CO | D. | 同体积、同密度的CO2和N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- | |
| B. | 金属钠跟水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ | |
| D. | 用醋酸除水垢(主要成分为碳酸钙):2H++CO32-=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠的摩尔质量为40g | |
| B. | 1摩尔氧原子的质量就是氧的相对原子质量 | |
| C. | H2SO4的摩尔质量为96g•mol-1 | |
| D. | 1molCO2的质量以克为单位时,在数值上等于CO2的相对分子质量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com