
已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是285.8kJ•mol﹣1、1411.0kJ•mol﹣1和1366.8kJ•mol﹣1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为()
A. ﹣44.2 kJ•mol﹣1 B. +44.2 kJ•mol﹣1
C. ﹣330 kJ•mol﹣1 D. +330 kJ•mol﹣1
考点: 用盖斯定律进行有关反应热的计算.
专题: 化学反应中的能量变化.
分析: 由燃烧热的概念写出各反应的热化学方程式,利用盖斯定律计算.
解答: 解:已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是﹣285.8kJ/mol、﹣1411.0kJ/mol和﹣1366.8kJ/mol,则有:①H2(g)+ O2(g)=H2O(l)△H=﹣285.8kJ/mol;
O2(g)=H2O(l)△H=﹣285.8kJ/mol;
②C2H4(g)+3O2(g)=2H2O(l)+2CO2(g)△H=﹣1411.0kJ/mol;
③C2H5OH(l)+3O2(g)=3H2O(l)+2CO2 (g)△H=﹣1366.8kJ/mol;
根据盖斯定律 ②﹣③可得:C2H4(g)+H2O(l)=C2H5OH(l)△H=﹣44.2kJ/mol,
故选A.
点评: 本题考查反应热的计算,题目难度中等,注意盖斯定律应用于反应热的计算.


科目:高中化学 来源: 题型:
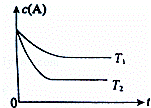
反应A(g)⇌B(g)+C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L.温度T1和T2下A的浓度与时间关系如右图所示.回答下列问题:
(1)上述反应的温度T1小于 T2,平衡常数K(T1) K(T2).(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为 .
②反应的平衡常数K= .
③反应在0~5min区间的平均反应速率v(A)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
把500mL有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则原混合溶液中钾离子物质的量浓度为( )
|
| A. | 0.1(b﹣2a)mol/L | B. | 10(2a﹣b)mol/L | C. | 10(b﹣a)mol/L | D. | 10(b﹣2a)mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学变化中的能量关系的说法中,错误的是()
A. 任何一个化学变化的过程中都包含着能量的变化
B. 化学变化过程中能量变化的实质就是旧键断裂要吸收能量,新键生成会放出能量
C. 如果生成物的能量比反应物的能量高,则该反应为放热反应
D. 如不特别注明,化学反应的反应热就是就是该反应的焓变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解精炼铜的说法中错误的是()
A. 粗铜做正极
B. 电解一段时间后,溶液中会存在锌、铁等不活泼的金属阳离子
C. 阳极泥中含有金、银等贵重金属
D. 电解质溶液可以选用硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨电极电解足量M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的相对原子质量为()
A. 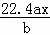 B.
B.  C.
C. 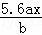 D.
D. 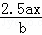
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生设计的用氨催化法制取少量HNO3溶液的实验装置如图所示: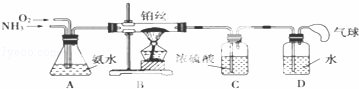
(1)实验室制备NH3,下列方法中适宜选用的是 (填序号).
①固态氯化铵与熟石灰混合加热
②固态氯化铵加热分解
③碱石灰中滴加浓氨水
④氯化铵溶液与氢氧化钠溶液共热
(2)装置B中发生反应的化学方程式为 .在实验过程中,加热铂丝红热后,移去酒精灯,发现铂丝还继续保持红热,由此可判断该反应是 (填“吸热”或“放热”)反应.
(3)装置C的作用是 ;装置C中的现象是 ;为确保装置D中尽可能多地生成HNO3,所通入O2和NH3的体积比应大于 .
(4)装置D中发生的反应方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
1L某混合溶液中,溶质X、Y的浓度都为0.1mol•L﹣1,向混合溶液中滴加某溶液Z(0.1mol•L﹣1氢氧化钠或硫酸溶液)至溶液呈中性,所得沉淀的物质的量如图所示,则X、Y、Z分别是( )
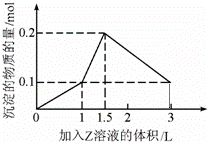
|
| A. | 氯化铝、氯化铁、氢氧化钠 | B. | 氯化铝、氯化镁、氢氧化钠 |
|
| C. | 偏铝酸钠、氢氧化钡、硫酸 | D. | 偏铝酸钠、氯化钡、硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com