
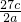
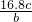
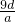
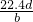
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
Al2O3+![]() 2AlN+3CO
2AlN+3CO
由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验:
(1)称取
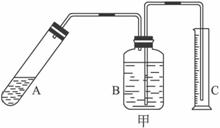
①上述反应的化学方程式为___________________________________。
②该样品中的AlN的质量分数为_______________。
③在装置B中所选择的试剂是________________(填序号)。
a.H2O b.浓H2SO
④上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列乙、丙两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数。较合理的装置是___________(填代号)。
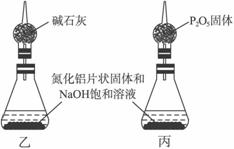
(2)另取
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市浦东新区高三下学期二模化学试卷(解析版) 题型:选择题
将a g铝粉加入过量NaOH溶液中充分反应后,铝粉完全溶解,并收集到标准状况下b L氢气,所得溶液中共有c个溶质离子,反应中转移电子d个。则阿伏加德罗常数(NA)可表示为
A. B.
B.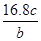 C.
C.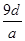 D.
D.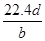
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市浦东新区高三4月高考预测(二模)化学试卷(解析版) 题型:选择题
将a g铝粉加入过量NaOH溶液中充分反应后,铝粉完全溶解,并收集到标准状况下b L氢气,所得溶液中共有c个溶质离子,反应中转移电子d个。则阿伏加德罗常数(NA)可表示为
A.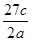 B.
B.
C.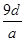 D.
D.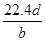
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com