
| A. | Na+、OH-、HS-NO3- | B. | Al3+、Cl-、HCO3-、Na+ | ||
| C. | AlO2-、K+、CO32-、Na+ | D. | Fe2+、K+、H+、NO3- |
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液,则离子方程式为:HA-+OH-=A2-+H2O | |
| B. | 室温时,1.0L、pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| C. | 由水电离出的c(H+)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=NH3•H2O+Al(OH)3↓+2BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
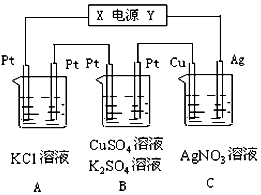
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
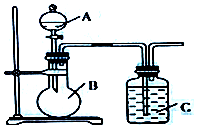
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
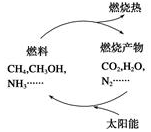 能量是当今社会发展的三大支柱之一.利用太阳能让燃料的燃烧产物如CO2、H2O、N2等重新组合,从而实现如图所示的转化.在此物质循环中太阳能转化为( )
能量是当今社会发展的三大支柱之一.利用太阳能让燃料的燃烧产物如CO2、H2O、N2等重新组合,从而实现如图所示的转化.在此物质循环中太阳能转化为( )| A. | 化学能 | B. | 核能 | C. | 机械能 | D. | 电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
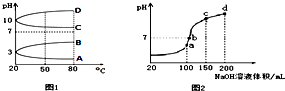 NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0 | B. | +3 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
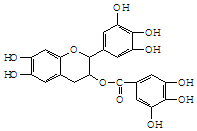 已知绿茶中含有EGCG,该物质具有抗癌作用,EGCG的结构简式如图所示,有关说法不正确的是( )
已知绿茶中含有EGCG,该物质具有抗癌作用,EGCG的结构简式如图所示,有关说法不正确的是( )| A. | 1molEGCG最多可与9mol H2发生加成反应 | |
| B. | 1molEGCG最多可与含6mol Br2的浓溴水反应 | |
| C. | EGCG在空气中易被氧化 | |
| D. | EGCG能与碳酸氢钠溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com