
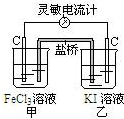
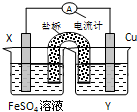
| A. | 反应开始时,乙中石墨电极上发生还原反应 | |
| B. | 反应开始时,甲中石墨电极上Fe3+被氧化 | |
| C. | 盐桥中的K+向乙中迁移,Cl-向甲中迁移 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为正极 |
分析 根据常温下能自动发生的氧化还原反应都可设计成原电池,再利用总反应2Fe3++2I-?2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的碳棒作正极,乙烧杯中的碳棒作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答.
解答 解:A.乙中I-失去电子放电,元素的化合价升高,发生氧化反应,所以乙中石墨电极上发生氧化反应,故A错误;
B.由总反应方程式知,Fe3+被还原成Fe2+,则甲中Fe3+发生还原反应,故B错误;
C.甲中碳棒为正极,电流从甲中碳棒流向乙中碳棒,则盐桥中的K+向甲中迁移,Cl-向乙中迁移,故C错误;
D.当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D正确;
故选D.
点评 本题考查原电池工作原理,并注重与化学平衡的联系,题目难度中等,明确原电池的工作原理、正负极的判断方法、化学平衡的影响因素为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4?2H++SO42- | B. | BaCl2═Ba2++2Cl- | ||
| C. | NH3•H2O═NH4++OH- | D. | Na2CO3═Na++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  除去粗盐溶液中的不溶物 | B. | 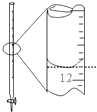 记录滴定终点读数为12.20ml | ||
| C. | 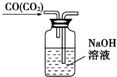 除去CO气体中的CO2气体 | D. | 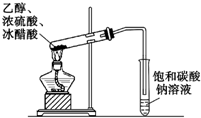 乙酸乙酯制备演示实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
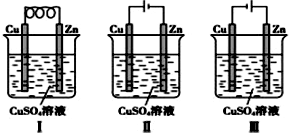
| A. | Ⅰ是原电池,Ⅱ是电镀装置 | |
| B. | Ⅰ、Ⅱ装置中锌极上均发生氧化反应 | |
| C. | Ⅱ、Ⅲ装置中,铜极均发生氧化反应而溶解 | |
| D. | Ⅱ、Ⅲ装置中Cu2+浓度基本不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Na+>N3->H+ | |
| B. | 氢铝化合物与水反应生成氢氧化铝和氢气 | |
| C. | 与盐酸反应都只生成一种盐 | |
| D. | 与水反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe在少量Cl2中燃烧生成FeCl2 | |
| B. | 石油的裂解、煤的干馏都是化学变化 | |
| C. | 化学反应的焓变与反应的途径有关 | |
| D. | 等质量的铜按a、b两种途径完全转化为硝酸铜,途径a、b消耗的硝酸一样多 途径a:Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀硝酸}{→}$Cu(NO3)2;途径b:Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③④⑥ | C. | ①②③④⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com