
【题目】现有以下物质:①食盐水 ②二氧化碳 ③盐酸 ④蔗糖 ⑤硫酸氢钠固体 ⑥氧气 ⑦纯醋酸 ⑧金属铜 ⑨碳酸氢钠固体。请回答下列问题(用序号填写)
(1)能导电的是________________________,属于电解质的是___________________,属于非电解质的是____________________。
(2)写出相关电解质在水溶液中的电离方程式_____________________________________________________________
【答案】①③⑧⑤⑦⑨②④CH3COOH![]() CH3COO-+H+ NaHCO3=Na++HCO3- NaHSO4=Na++H++SO42-
CH3COO-+H+ NaHCO3=Na++HCO3- NaHSO4=Na++H++SO42-
【解析】
①食盐水含有自由移动离子,导电,属于混合物,不是电解质,也不是非电解质;
②二氧化碳不含有自由电子和自由移动离子,不导电,属于非电解质;
③盐酸含有自由移动离子,导电,属于混合物,不是电解质,也不是非电解质;
④蔗糖不含有自由电子和自由移动离子,不导电,水溶液里和熔融状态下都不能导电,属于非电解质;
⑤硫酸氢钠固体属于电解质,在固态不导电,在熔融状态下可以导电;
⑥氧气不含有自由电子和自由移动离子,不导电,属于单质,不是电解质,也不是非电解质;
⑦纯醋酸,不含有自由电子和自由移动离子,不导电,水溶液里能够导电,属于电解质;⑧熔融的硫酸钾含有自由移动的离子,能够导电,属于电解质;
⑧金属铜含有自由电子,导电,属于单质,不是电解质,也不是非电解质;
⑨碳酸氢钠固体不含有自由电子和自由移动离子,不导电,水溶液里和熔融状态下能导电,属于电解质;
所以:
(1)以上物质能导电的是:①③⑧,
故答案为:①③⑧;
(2)以上物质属于电解质的是:⑤⑦⑨;以上物质属于非电解质的是:②④,
故答案为:⑤⑦⑨;②④;
(3)⑤硫酸氢钠在水中完全电离,电离方程式为:NaHSO4=Na++H++SO42-
⑦纯醋酸水溶液中电离为弱电解质, CH3COOH![]() CH3COO-+H+,
CH3COO-+H+,
⑨碳酸氢钠固体溶液中电离出碳酸氢根离子和钠离子,电离方程式为:NaHCO3=Na++HCO3-
故答案为: NaHSO4=Na++H++SO42-;CH3COOH![]() CH3COO-+H+;NaHCO3=Na++HCO3-
CH3COO-+H+;NaHCO3=Na++HCO3-


科目:高中化学 来源: 题型:
【题目】标准状况下,有以下三种物质:①18 g H2O;②11.2 L H2S气体;③0.5 mol C2H5OH(酒精)。下列排列顺序正确的是
A. 密度:①>③>② B. 体积:①>③>②
C. 质量:③>②>① D. 氢原子数:①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.
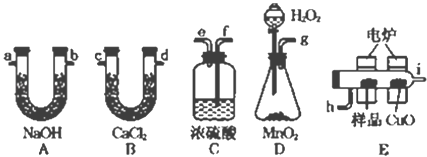
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g→ → →h→i→ → → → ._______________
(2)燃烧管中CuO的作用是______.
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取3.24g样品,经充分反应后,A管质量增加9.24g,B管质量增加2.16g,则该样品的实验式为______.
(4)要确定该物质的分子式,还要知道该物质的______.经测定其蒸气密度为4.82g/L(已换算为标准状况下),则其分子式为______.
(5)经红外光谱分析知该化合物的分子中存在1个苯环,苯环上只有1个支链,且支链中有1个甲基.试写出该有机物的结构简式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原子的电子排布式为1s22s22p63s23p63d54s2 , 下列说法中不正确的是( )
A.该元素原子中共有25个电子
B.该元素原子核外有4个能层
C.该元素原子最外层共有2个电子
D.该元素原子M电子层共有8个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z的原子序数依次增大,WX2 为红棕色气体,Y的单质既能与强酸又能与强碱反应,W、Z 最外层电子数之和是X最外层电子数的2 倍。下列说法中错误的是
A. Y 与X、Y与Z均形成离子化合物
B. 对应简单离子的半径:W>X>Y
C. Z 对应的最高价含氧酸是一元强酸
D. ZX2 是一种消毒能力强于氯气且更加安全的自来水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色农药——信息素的推广使用,对环保有重要意义。有一种信息素的结构简式为![]() 。下列关于检验该信息素中官能团的试剂和顺序正确的是( )
。下列关于检验该信息素中官能团的试剂和顺序正确的是( )
A. 先加入酸性高锰酸钾溶液,后加银氨溶液,水浴加热
B. 先加入溴水,后加酸性高锰酸钾溶液
C. 先加入新制氢氧化铜悬浊液,加热,酸化后再加入溴水
D. 先加入银氨溶液,再另取该物质加入溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是
A. 有CO、CO2、O3三种气体,它们各含有1 mol O,则三种气体物质的量之比为3:2:1
B. n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为35.5m/n
C. 常温下,a L氧气和氮气的混合物含有的分子数就是(a/22.4)×6.02×1023个
D. 28 g CO和22.4 L CO2中含有的碳原子数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释. 100 倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为________ mol·L1(计算结果保留 2位有效数字)。
(2)某同学取 100mL 该“84消毒液” ,稀释后用于消毒,稀释后的溶液中n(Na+)=_______ mol.
(3)“84消毒液”与稀硫酸混合用可增强消毒能力,某消毒小组用98%(ρ=1.84g·cm-3)的浓硫酸配制2L 2.3mol·L-1的稀硫酸,用于增强“84消毒液”的消毒能力,需用浓硫酸的体积为_______mL。
(4)“84消毒液”与“洁厕灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。实验室用密度为1.25 g·mL-1,质量分数36.5%的浓盐酸配制0.1 mol·L-1的盐酸240 mL。
①配制240 mL 0.1 mol·L-1的盐酸应选用______mL的容量瓶。
②下列操作对所配溶液的浓度有何影响 (填“偏大”、“偏小”或“无影响”)。
A.定容时,俯视刻度线,浓度 ____________ ;
B.用量筒量取浓盐酸时,仰视刻度线,浓度 __________ ;
C.定容摇匀后发现溶液凹面低于刻度线,加水至刻度线,浓度 ____________ 。
D.容量瓶在使用前未干燥,里面有少量蒸馏水, 浓度 ____________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com