
·ÖĪö £Ø1£©Ńõ»ÆĪļŹĒŗ¬Į½ÖÖŌŖĖŲĘäÖŠŅ»ÖÖĪŖŃõŌŖĖŲµÄ»ÆŗĻĪļ£»
µē½āÖŹŹĒĖ®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀÄܵ¼µēµÄ»ÆŗĻĪļ£¬Ė®ČÜŅŗÖŠŗĶČŪȌדĢ¬ĻĀ¶¼²»µ¼µēµÄ»ÆŗĻĪļĪŖ·Ēµē½āÖŹ£»
»ģŗĻĪļŹĒ²»Ķ¬ĪļÖŹ×é³ÉµÄĪļÖŹ£¬ŅĄ¾ŻøÅÄī·ÖĪöŃ”ĻīÖŠµÄĪļÖŹ£»
£Ø2£©øł¾Żn=$\frac{V}{{V}_{m}}$¼ĘĖćĪļÖŹµÄĮ棬ŅĄ¾ŻĆܶČŗĶČÜŅŗÖŹĮæ¼ĘĖćČÜŅŗĢå»ż£¬V=$\frac{m}{¦Ń}$£¬øł¾Żc=$\frac{n}{V}$¼ĘĖćĪļÖŹµÄĮæÅØ¶Č£»
£Ø3£©Ļņ·ŠĖ®ÖŠµĪČė¼øµĪ±„ŗĶFeCl3ČÜŅŗ£¬¼ĢŠųÖó·ŠÖĮČÜŅŗ³ŹŗģŗÖÉ«£¬¼“ÖʵĆFe£ØOH£©3½ŗĢ壬ĒāŃõ»ÆĢś½ŗĢåµĪČėĮņĖįĻČ¾Ū³ĮÉś³É³ĮµķĒāŃõ»ÆĢś£¬¼ĢŠųµĪČėĮņĖį£¬ĒāŃõ»ÆĢś³ĮµķČܽā£»
½ā“š ½ā£ŗ£Ø1£©¢ŁNaCl¾§ĢåŹĒ“æ¾»µÄ»ÆŗĻĪļ£¬Ė®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀÄܵ¼µē£¬ŹōÓŚµÄµē½āÖŹ£»
¢ŚøɱłŹĒ¹ĢĢ嶞Ńõ»ÆĢ¼£¬ŹōÓŚŃõ»ÆĪļ£¬ČÜÓŚĖ®Éś³Éµē½āÖŹĢ¼Ėį£¬±¾Éķ²»ÄܵēĄė³öĄė×ÓŹōÓŚ·Ēµē½āÖŹ£»
¢Ū°±Ė®ŹĒ°±ĘųµÄĖ®ČÜŅŗ£¬ŹĒŅ»ÖÖ·ÖÉ¢ĻµŹōÓŚ»ģŗĻĪļ£»
¢ÜĶŹĒµ„ÖŹ£¬¼Č²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ£»
¢ŻBaSO4¹ĢĢåŹĒŃĪ£¬ČŪȌדĢ¬ĻĀÄܵ¼µēŹōÓŚµē½āÖŹ£»
¢ŽŅŅ“¼ŹĒÓŠ»śĪļ£¬±¾Éķ²»ÄܵēĄė³öĄė×Ó£¬ŹōÓŚ·Ēµē½āÖŹ£»
¢ßČŪČŚµÄKNO3µ¼µē£¬ŹĒ“æ¾»µÄ»ÆŗĻĪļŹōÓŚµē½āÖŹ£»
¢ąĻ”ĮņĖįŹĒĮņĖįµÄĖ®ČÜŅŗ£¬ŹĒŅ»ÖÖ·ÖÉ¢ĻµŹōÓŚ»ģŗĻĪļ£»
ĖłŅŌŹōÓŚŃõ»ÆĪļµÄĪŖ¢Ś£¬ŹōÓŚµē½āÖŹµÄĪŖ¢Ł¢Ż¢ß£¬ŹōÓŚ»ģŗĻĪļµÄ¢Ū¢ą£¬
¹Ź“š°øĪŖ£ŗ¢Ś£¬¢Ł¢Ż¢ß£¬¢Ū¢ą
£Ø2£©n£ØHCl£©=$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol£¬
ČÜŅŗµÄ×ÜÖŹĮæĪŖ1100g
ČÜŅŗµÄĢå»żĪŖ£ŗV£ØČÜŅŗ£©=$\frac{m}{¦Ń}$=$\frac{1100g}{1.1g/ml}$=1000ml£¬¼“1L£¬
Ōņ£ŗc=$\frac{n}{V}$=$\frac{\frac{V}{22.4}mol}{1L}$=$\frac{V}{22.4}$mol/L£¬
¹Ź“š°øĪŖ£ŗ$\frac{V}{22.4}$£»
£Ø3£©ŹµŃéŹŅÖʱøĒāŃõ»ÆĢś½ŗĢåŹĒŌŚ·ŠĢŚµÄÕōĮóĖ®ÖŠ¼ÓČė±„ŗĶĀČ»ÆĢśČÜŅŗ£¬µ±ČÜŅŗ±äĪŖŗģŗÖÉ«Ź±Į¢¼“Ķ£Ö¹¼ÓČČ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗFeCl3+3H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$ Fe£ØOH£©3£Ø½ŗĢ壩+3HCl£¬ĻņFe£ØOH£©3½ŗĢåÖŠÖšµĪ¼ÓČė¹żĮæµÄĻ”ĮņĖį£¬½ŗĢåŌŚµē½āÖŹČÜŅŗÖŠŅõŃōĄė×Ó×÷ÓĆĻĀ²śÉś¾Ū³ĮĻÖĻó£¬ÓŠŗģŗÖÉ«³ĮµķÉś³É£¬¼ĢŠųµĪČėĮņĖįŗóĒāŃõ»ÆĢśÓÖŗĶĮņĖį·“Ӧɜ³ÉĖ®ŗĶæÉČÜŠŌµÄĮņĖįĢś£¬ĖłŅŌĻÖĻóĪŖ£ŗæŖŹ¼µĪ¼ÓŹ±ÓŠŗģŗÖÉ«³Įµķ³öĻÖ£¬¼ĢŠųµĪ¼Ó³ĮµķČܽā£¬
¹Ź“š°øĪŖ£ŗFeCl3+3H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$Fe£ØOH£©3£Ø½ŗĢ壩+3HCl£¬æŖŹ¼µĪ¼ÓŹ±ÓŠŗģŗÖÉ«³Įµķ³öĻÖ£¬¼ĢŠųµĪ¼Ó³ĮµķČܽā£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹ·ÖĄą·½·Ø£¬ĪļÖŹ×é³ÉŗĶĆū³Ę£¬ČÜŅŗÅØ¶ČµÄ¼ĘĖćŗĶ½ŗĢåÖʱøµÄÓ¦ÓĆ£¬×¢ŅāøÅÄīŹµÖŹĒų±šŗĶ½ŗĢåŠŌÖŹµÄĄķ½āÓ¦ÓĆ£¬ĢāÄæ½Ļ¼ņµ„£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŠņŗÅ | A | B | C |
| ×°ÖĆ | 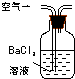 | 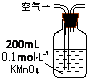 | 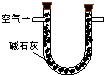 |
| ŌĄķ | ĶØČėVÉżæÕĘų£¬²ā¶ØÉś³É³ĮµķµÄÖŹĮæ | µ±KMnO4ČÜŅŗøÕŗĆĶŹÉ«Ź±£¬²ā¶ØĶØČėæÕĘųµÄĢå»żV | ĶØČėVÉżæÕĘų£¬²ā¶ØUŠĶ¹ÜŌö¼ÓµÄÖŹĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.06mol/L | B£® | 0.12mol/L | C£® | 0.03mol/L | D£® | 0.24mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.7 g | B£® | 5.4 g | C£® | 6.75 g | D£® | 8.1 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
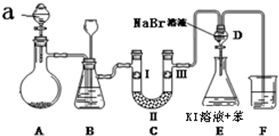
| a | b | c | d | |
| I | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ |
| ¢ņ | ¼īŹÆ»Ņ | ¹č½ŗ | ĪŽĖ®ĀČ»ÆøĘ | ÅØĮņĖį |
| ¢ó | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŹµŃéŹŅÓĆÅű„ŗĶŹ³ŃĪĖ®Ą“ŹÕ¼ÆĀČĘų | B£® | ĻÄĢģµÄŹ³ĪļøüŅ×øÆŹ“ | ||
| C£® | °±Ė®ŹŹŅĖ±£“ęŌŚµĶĪĀ“¦ | D£® | “×ĖįÄÜÓĆĄ“ĒåĻ“Ė®¹ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÉĻŹö×ĘÉÕ¹ż³ĢµÄĪ²Ęų¾łæÉÖ±½ÓÅŵ½æÕĘųÖŠ | |
| B£® | ÓÉ6 mol CuFeS2Éś³É6 mol Cu£¬ÉĻŹö¹²ĻūŗÄ15 mol O2 | |
| C£® | ŌŚ·“Ó¦2Cu2O+Cu2SØT6Cu+SO2ÖŠ£¬×÷Ńõ»Æ¼ĮµÄÖ»ÓŠCu2O | |
| D£® | µē½ā¾«Į¶Ź±£¬“ÖĶÓ¦ÓėĶāµēŌ“Õż¼«ĻąĮ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
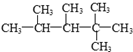 ŹĒÓÉŅ»ÖÖµ„Ļ©Ģž¼ÓĒā¶ų³ÉµÄ£¬ÄĒĆ“ŌĻ©ĢžµÄæÉÄܽį¹¹ÓŠ£Ø””””£©
ŹĒÓÉŅ»ÖÖµ„Ļ©Ģž¼ÓĒā¶ų³ÉµÄ£¬ÄĒĆ“ŌĻ©ĢžµÄæÉÄܽį¹¹ÓŠ£Ø””””£©| A£® | 1ÖÖ | B£® | 2ÖÖ | C£® | 3ÖÖ | D£® | 4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molŅŅČ²·Ö×ÓĖłŗ¬µÄ¹²ÓƵē×Ó¶Ō×ÜŹżĪŖ5NA | |
| B£® | 1 mol¼×»ł£Ø-CH3 £©Ėłŗ¬µÄµē×Ó×ÜŹżĪŖ9NA | |
| C£® | 0.5 mol 1£¬3-¶”¶žĻ©·Ö×ÓÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü×ÜŹżĪŖNA | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4L¼ŗĶéĶźČ«Č¼ÉÕĖłÉś³ÉµÄĘųĢ¬²śĪļµÄ·Ö×ÓŹżĪŖ7NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com