
| 144g×(b-a)g |
| 16g |
| 9(b-a)g |
| ag |
| 9(b-a) |
| a |
| 9(b-a) |
| a |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
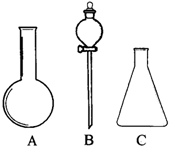 (1)有如图所示A、B、C三种仪器:请选择下列仪器名称的序号,填入相应的空格内:①烧杯②普通漏斗③圆底烧瓶④锥形瓶⑤分液漏斗⑥酸式滴定管
(1)有如图所示A、B、C三种仪器:请选择下列仪器名称的序号,填入相应的空格内:①烧杯②普通漏斗③圆底烧瓶④锥形瓶⑤分液漏斗⑥酸式滴定管查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法,化合物 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 的名称是2,2,4,5-四甲基-3,3-二乙基己烷 |
| B、等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等 |
| C、苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
D、结构片段为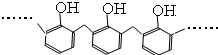 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:
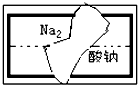 某中学学习小组在帮助老师整理实验室的化学试剂时,发现一盛有白色固体的试剂瓶,标签破损(如图),请你根据已掌握的知识,对该药品可能是什么物质作出猜想(4种),并设计实验验证.
某中学学习小组在帮助老师整理实验室的化学试剂时,发现一盛有白色固体的试剂瓶,标签破损(如图),请你根据已掌握的知识,对该药品可能是什么物质作出猜想(4种),并设计实验验证.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用电池外壳的金属材料 |
| B、防止电池中汞、镉、铅等重金属离子对土壤和水源的污染 |
| C、回收其中的石墨电极 |
| D、不使电池中渗出的电解液腐蚀其他物品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com