
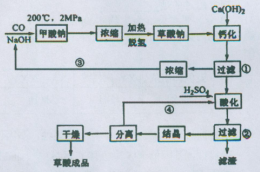


 。
。

 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源:不详 题型:单选题
| A.BaCl2 | B.Ba(OH)2 | C.Ba(NO3)2 | D.NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验:
、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验:
| A.现象3不能证明X中是否含有SO42— |
| B.现象2气体C中至少有一种是CO2或SO2,操作Ⅰ为过滤 |
C.现象5表明X溶液中一定含有Cl |
| D.现象1表明X溶液显酸性,沉淀D为Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过浓硫酸除去HCl中的H2O | B.通过灼热的CuO除去H2中的CO |
| C.通过灼热的镁粉除去N2中的O2 | D.通过水除去CO中的CO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
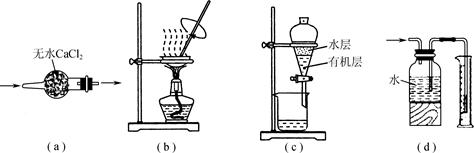
| A.用图a所示装置干燥SO2气体 |
| B.用图b所示装置蒸发CH3COONa溶液得醋酸钠晶体 |
| C.用图c所示装置分离有机层与水层,水层从分液漏斗下口放出 |
| D.用图d所示装置测量氯气的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.提高高锰酸钾的氧化能力,用浓盐酸酸化 |
| B.抑制Fe2+的水解,用稀硝酸酸化 |
| C.检验某卤代烃中是否含氯元素,先加HNO3酸化,再加AgNO3溶液检验 |
| D.确认溶液中含有SO42-时,先用盐酸酸化,再加BaCl2溶液检验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用溴水鉴别苯和正已烷 |
| B.用BaCl2溶液鉴别SO42﹣与SO32﹣ |
| C.用浓HNO3与Cu反应制备NO2 |
| D.将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
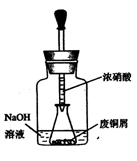
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com