
下列物质间的反应,其能量变化符合下图的是( )

A.由Zn和稀H2SO4制氢气
B.灼热的炭粉与二氧化碳反应
C.Ba(OH)2·8H2O晶体和NH4Cl晶体混合
D.碳酸钙的分解
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:2016-2017学年天津静海一中等六校高一上期中化学卷(解析版) 题型:选择题
下列溶液中,能大量共存的离子组是 ( ) 、
A.遇酚酞试剂变红的溶液:K+、Cu2+、NO3-、SO42-
B.遇紫色石蕊试剂变红的溶液:K+、Na+、Cl-、CO32-
C.常温pH<7的溶液:Ba2+、NH4+、NO3-、Cl-
D.无色透明溶液中:K+、Na+、MnO4-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
下列对熵的理解不正确的是( )
A.同种物质气态时熵值最大,固态时熵值最小
B.体系越有序,熵值越小;越混乱,熵 值越大
值越大
C.与外界隔离的体系,自发过程将导致体系的熵减小
D.25 ℃、1.01×105  Pa时,2N2O5(g)=4NO2(g)+O2(g)是熵增的反应
Pa时,2N2O5(g)=4NO2(g)+O2(g)是熵增的反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是( )
A.2v(NH3)=v(CO2) B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:填空题
(1)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全剂而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
方法一
① 氧化剂 、氧化产物 、
②氧化剂与还原剂物质的量比 。
③用双线桥法标明电子转移的方向和数目
方法二
④被氧化的物质是 ________
⑤若反应中有0.1 mol电子转移,则产生的ClO2气体在标准状况下的体积为________L;
(2)某无色透明溶液与金属铝反应放出H2,试判断下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-哪些能大量共存。
⑥当生成Al3+ 时,可能存在 _。
⑦当生成AlO2- 时,可能存在 _。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
将等物质的量的Na2O和Na2O2分别投入到足量且等质量的水中 ,得到溶质质量分数分别为
,得到溶质质量分数分别为 %和
%和 %的两种溶液,则
%的两种溶液,则 和
和 的关系是( )
的关系是( )
A. >
> B.
B. =
= C.
C. <
< D.无法确定
D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上月考二化学卷(解析版) 题型:选择题
高铁酸钾(K2FeO4)是一种高效绿色水处理剂,其工业制备的反应原理为:2F(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O,下列说法正确的是( )
A.制高铁酸钾用KClO做还原剂
B.KCl是还原产物
C.高铁酸钾中铁的化合价为+7
D.制备高铁酸钾时1molFe (OH)3得到3 mol电子
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷(解析版) 题型:实验题
甲乙两同学分别对含+4价硫元素的物质性质进行了探究。
(1)甲用右图装置进行实验(气密性已检验,加热和夹持装置已略去)。实验进行一段时间后,C、D中都出现明显的白色沉淀,经检验均为BaSO4。
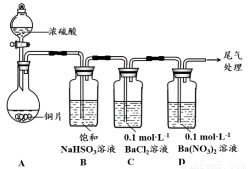
① A中反应的化学方程式是 。
② 为探究SO2在D中所发生的反应,甲进一步实验发现,出现白色沉淀的过程中,D溶液中NO3-浓度几乎不变。 甲据此得出结论:D中出现白色沉淀的主要原因是 。
(2)乙用如下实验对含+4价硫元素的物质性质继续进行探究。
序号 | 实验操作 | 实验现象 |
1 | 取0.3 g 纯净Na2SO3固体,向其中加入10 mL 2 mol·L-1 盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,4 min后,溶液变浑浊 |
2 | 取0.3 g 纯净Na2SO3固体,向其中加入10 mL 2 mol·L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2 h后,溶液变浑浊 |
3 | 取0.3 g 纯净Na2SO3固体,向其中加入10 mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
结合化学用语解释实验1中产生现象的原因: ; 。
由实验1、2、3对比,可以得到推论: 。
③ 乙通过查阅 资料发现,Na+对实验1和2中出现浑浊的时间无影响,于是进一步探究Cl-和NO3-对其的影响:
资料发现,Na+对实验1和2中出现浑浊的时间无影响,于是进一步探究Cl-和NO3-对其的影响:
序号 | 实验操作 | 实验现象 |
4 | 取 固体混合物,向其中加入10 mL 2 mol·L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,20 min后,溶液变浑浊 |
i.实验2和4对比,乙获得推论:Cl-的存在可以加快溶液中+4价硫元素的氧化;
ii.实验1和4对比,乙获得推论: 。
④ 通过以上实验,乙同学认为,确定某溶液中含有SO42-的实验方案:取待测液,向其中先滴加 (填字母序号)。
a.2 mol·L-1盐酸,再滴加BaCl2溶液,一段时间后出现白色沉淀
b.2 mol·L-1盐酸,再滴加BaCl2溶液,立即出现白色沉淀
c.2 mol·L-1硝酸,再滴加BaCl2溶液,一段时间后出现白色沉淀
d.2 mol·L-1硝酸,再滴加BaCl2溶液,立即出现白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com