
| 13.44L |
| 22.4L/mol |
| v |
| vm |
| 13.44L |
| 22.4L/mol |
| m |
| M |
| 5.8g |
| 58g/mol |
| n |
| v |
| 0.1mol |
| 0.1L |
| m |
| M |
| 15.6g |
| 78g/mol |
| 0.4mol |
| 4 |
| n |
| v |
| 0.3mol |
| 0.1L |
| n |
| v |
| 1.1mol |
| 0.1L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
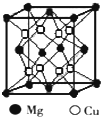 人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农业生产及日常生活方面用途非常广泛.试回答下列问题.
人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农业生产及日常生活方面用途非常广泛.试回答下列问题.| 丁炔铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
13 6 |
39 19 |
40 20 |
12 6 |
14 7 |
40 18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
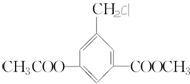 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )| A、该物质能发生消去反应 |
| B、苯环上的一氯代物有2种 |
| C、含有一种含氧官能团 |
| D、分子式是C10H12O4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH4+Cl2
| ||
B、2CH3CHO+O2
| ||
| C、CHCl3+HF→CHFCl2+HCl | ||
D、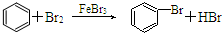 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.02 mol |
| B、0.01 mol |
| C、0.04 mol |
| D、无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com