
| A. | 熟石灰与水混合成糊状后会很快凝固,转化为坚硬的生石膏,可用它制作石膏绷带 | |
| B. | 人造纤维是利用自然界的非纤维材料通过化学合成方法得到的 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料,可减少“白色污染” |
分析 A、熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏.利用石膏的这一性质,人们常利用各种模型和医疗上用的;
B、以天然纤维素纤维(树皮、纸浆、废棉纱)为原料熔融纺丝、纺纱制造的,都是人造纤维;石油化工为原料制造的,都是合成纤维;
C.雾分散剂是空气,分散质为灰尘颗粒,活性炭具有吸附作用;
D.白色污染是指不能降解的聚乙烯塑料.
解答 解:A、熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏.利用石膏的这一性质,人们常利用各种模型和医疗上用的,故A正确;
B.以天然纤维素纤维(树皮、纸浆、废棉纱)为原料熔融纺丝、纺纱制造的,都是人造纤维,以石油化工为原料制造的,都是合成纤维,故B错误;
C.具有吸附性,能吸附异味、有毒物质和色素等,带活性炭口罩防雾霾是利用了活性炭具有吸附性,能吸附可吸入性颗粒物等,是吸附原理,故C正确;
D.利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代不能降解的聚乙烯塑料,可减少白色污染,故D正确;
故选B.
点评 本题考查了石膏性质应用,人造纤维和合成纤维的定义,白色污染、雾霾的理解应用,注意知识的积累,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1.8 g | B. | 2.7 g | C. | 4.05g | D. | 5.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
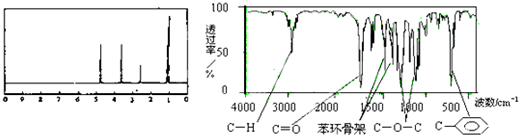
| A. | A分子属于酯类化合物,在一定条件下能发生水解反应 | |
| B. | 符合题中A分子结构特征的有机物有两种 | |
| C. | A在一定条件下可与3 mol H2发生加成反应 | |
| D. | 分子式为C8H8O2且分子中含苯环和-COOR(-R为烃基)的物质共有6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F 是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去):
A、B、C、D、E、F 是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去): .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
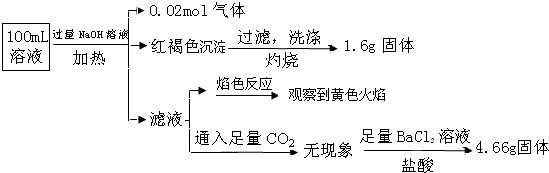
| A. | 原溶液中c(Fe3+)=0.2 mol•L-1 | |
| B. | 溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol•L-1 | |
| C. | SO42ˉ、NH4+、Na+一定存在,CO32ˉ、Al3+一定不存在 | |
| D. | 要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2014年德美科学家因开发超分辨率荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代.利用此类光学显微镜可以观察活细胞内蛋白质等大分子 | |
| B. | 能量是可以互相转化的.植物的光合作用可将太阳能转变成化学能,单晶硅可将光能转变成电能.原电池和电解池可实现化学能和电能的相互转换 | |
| C. | 分类方法、统计方法、定量研究、实验方法和模型化方法等是化学研究的常用方法 | |
| D. | 利用外接直流电源保护铁质建筑物,属于电化学中牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
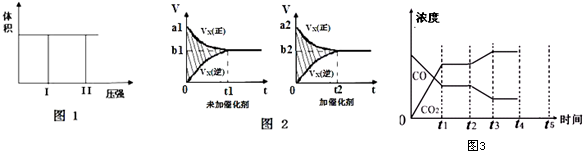
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取操作中,分液漏斗振摇后需要放气,放气的具体操作为,将分液漏斗置于铁架台的铁圈上,打开上口玻璃塞 | |
| B. | 燃料电池制作中,为了能吸附更多气体,在两根碳棒表面包上一层薄海绵 | |
| C. | 用硫代硫酸钠溶液和硫酸溶液反应测反应速率是实验中,可以通过判断气泡多少来比较反应速率快慢 | |
| D. | 酸碱中和滴定操作中,用酸润洗过的滴定管需要用蒸馏水再润洗一次 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com