
| A. | 人体内氨基酸的分解代谢最终产物是水、二氧化碳和尿素 | |
| B. | 构成蛋白质的氨基酸分子的结构通式可以表示为: | |
| C. | 氨基酸只能和碱反应不能和酸反应 | |
| D. | 两个氨基酸通过脱水缩合形成二肽 |
分析 A.氨基酸含有碳氢氧氮元素;
B.构成天然蛋白质的氨基酸分子为α-氨基酸;
C.氨基酸含有氨基和羧基,显两性;
D.两个氨基酸通过脱水缩合以后形成二肽.
解答 解:A.人体内氨基酸的代谢终产物是水、二氧化碳和尿素,故A正确;
B.生物体蛋白质的基本组成单位是α-氨基酸,α-氨基酸的结构特点是有一个氨基和一个羧基同时连在同一个碳原子上,结构通式是 ,故B正确;
,故B正确;
C.基酸含有氨基和羧基,显两性,既能与酸反应又能与碱反应,故C错误;
D.两个氨基酸通过脱水缩合以后形成的化合物叫做二肽,故D正确.
故选C.
点评 本题考查氨基酸、蛋白质的结构性质及在人体内转化,难度较小,旨在考查学生对基础知识的掌握.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 阳极:Cu-2e-═Cu2+ 阴极:Cu2++2e-═Cu | |
| B. | 阳极:2Cu+2I--2e-═2CuI 阴极:2H++2e-═H2↑ | |
| C. | 阳极:2I--2e-═I2 阴极:2H++2e-═H2↑ | |
| D. | 阳极:4OH--4e-═2H2O+O2↑ 阴极:4H++4e-═2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.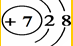 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(OH-)>10-7 mol•L-1的溶液一定呈碱性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(H+)=c(OH-)的溶液一定呈中性 | |
| D. | 不能使酚酞试液变红的溶液一定呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使燃料充分燃烧 | B. | 加大能源开采力度 | ||
| C. | 加强能源利用的科技投入 | D. | 合理使用能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com