
| ||
| ||
 ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、废弃的金属、纸制品、塑料是可回收资源,玻璃不是可回收资源 |
| B、大力推广农作物的生物防治技术,以减少农药的使用 |
| C、“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 |
| D、“低碳生活”倡导生活中耗用能量尽量减少从而减少CO2排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是生成盐和水的反应都是中和反应 |
| B、复分解反应可能是氧化还原反应 |
| C、生成一种单质和一种化合物的反应一定是置换反应 |
| D、有单质生成的分解反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
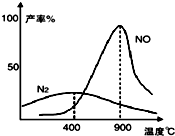 氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3溶于盐酸中:HCO3-+H+═H2O+CO2↑ |
| B、Na2O溶于盐酸中:O2-+2H+═H2O |
| C、Mg(OH)2溶于盐酸中:OH-+H+═H2O |
| D、CaCO3溶于盐酸中:CO32-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com