
【题目】2009年甲型H1N1流感席卷全球,引起了全世界人们的高度关注。金刚乙胺、达菲等药物可用于预防甲型H1N1流感。
(1)金刚乙胺是金刚乙烷的衍生物,其结构如图所示, 其分子式为:______________。
其分子式为:______________。
(2)金刚乙烷有很多一氯代物,A是其中之一。A有如下转化关系:

经检测:一个E分子中含有两个羰基,但与新制氢氧化铜悬浊液共热得不到砖红色沉淀;1 mol F与足量的钠完全反应生成22.4 L气体(换算成标况)。
试回答下列问题:(用“R”表示![]() )
)
①写出D、E的结构简式:D________________________,E_______________________。
②写出C→D的化学方程式:________________________________________________。
A→B、E→F的反应类型分别为:__________________、__________________。
③F在一定条件下,可发生反应形成高分子化合物I,I的结构简式为 ![]() 。试写出F中含氧官能团的名称:__________________________。
。试写出F中含氧官能团的名称:__________________________。
④金刚乙烷的一氯代物有________种。
【答案】 C12H21N R—CHOH—CH2OH ![]() R—CHBr—CH2Br+2H2O
R—CHBr—CH2Br+2H2O![]() 2HBr+R—CHOH—CH2OH 消去反应 还原反应(或加成反应) 羟基、羧基 5
2HBr+R—CHOH—CH2OH 消去反应 还原反应(或加成反应) 羟基、羧基 5
【解析】(1)由金刚乙胺结构可知,其分子式为C12H21N。
(2)由A生成B的条件(NaOH的乙醇溶液),可以推断这是一个卤代烃的消去反应,生成物B可能含有碳碳双键。B与Br2加成生成C,得到溴代烃,再经水解,即可得到二元醇D。由已知E分子中有两个C=O键,但与新制Cu(OH)2悬浊液共热得不到砖红色沉淀,可知E分子中无醛基,E只能为R—CO—COOH(R代表金刚烷基),由E可推出D为 R—CHOH—CH2OH。1 mol F与足量的钠完全反应生成22.4 L气体,说明F分子中有2个活泼H原子,所以F为R—CHOH—COOH。
①D的结构简式为 R—CHOH—CH2OH ,E的结构简式为 ![]() 。
。
②C→D的化学方程式为R—CHBr—CH2Br+2H2O![]() 2HBr+R—CHOH—CH2OH。
2HBr+R—CHOH—CH2OH。
A→B、E→F的反应类型分别为消去反应、还原反应(或加成反应)。
③F在一定条件下,可发生反应形成高分子化合物I,I的结构简式为 ![]() 。F中含氧官能团有羟基、羧基。
。F中含氧官能团有羟基、羧基。
④金刚乙烷的一氯代物有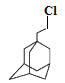 、
、 、
、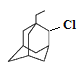 、
、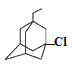 、
、 等5种。
等5种。


科目:高中化学 来源: 题型:
【题目】已知 ![]() H2(g)+
H2(g)+ ![]() C12(g)═HCl(g);△H=﹣92.3kJmol﹣1 , 则反应2HCl(g)═H2(g)+Cl2(g)的△H为( )
C12(g)═HCl(g);△H=﹣92.3kJmol﹣1 , 则反应2HCl(g)═H2(g)+Cl2(g)的△H为( )
A.+92.3 kJmol﹣1
B.﹣92.3 kJmol﹣1
C.﹣184.6 kJmol﹣1
D.+184.6 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习物质结构与性质的重要工具.下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素.请用所给元素回答下列问题.(均用元素符号填写)
(1)被选作相对原子质量标准的核素是(填写核素符号),B元素在元素周期表中的位置 .
(2)E、Q、R三种元素原子形成的简单离子具有相同电子层结构,其中半径最大的离子的是(填离子符号); 写出MD2分子的结构式: .
(3)选取两种元素,形成既含有离子键又含有共价键的化合物,该化合物电子式为;最高价氧化物的水化物中,酸性最强的化合物分子式为 .
(4)用表中所给元素组成反应物,请各用一个化学方程式说明:元素Q和R非金属性的强弱:;
元素G和H的金属性强弱: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在原子的第n电子层中,当它属于最外层电子层时,最多容纳的电子数目与n-1层相同,当它属于次外层时,最多容纳的电子数比n+1层最多容纳的电子数多10个电子,则此电子层是 ( )
A. K层 B. L层 C. M层 D. N层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2作为重要的燃料和化工原料,有着十分广泛的应用.
(1)已知:C(s)+O2(g)=CO2(g)△H1=﹣393.5kJmol﹣1C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJmol﹣1
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g)△H=kJmol﹣1 .
(2)利用反应CO(g)+H2(g)+O2(g)=CO2(g)+H2O(g)设计而成的MCFS燃料电池是用水煤气(CO和H2物质的量之比为1:1)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质的一种新型电池.现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置以及现象如图所示.则有:
①燃料电池即电源的N极的电极反应式为;
②已知饱和食盐水的体积为1L,一段时间后,测得左侧试管中气体体积为11.2mL(标准状况),若电解前后溶液的体积变化忽略不计,而且电解后将溶液混合均匀,则此时溶液的pH为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类的概念是( )
A. 含有碳、氢、氧三种元素的有机物
B. 有甜味的物质
C. 符合通式Cn(H2O)m的化合物
D. 一般是多羟基醛、多羟基酮以及能水解生成它们的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子浓度在指定溶液中一定能大量共存的是( ) ①加入铝能放出H2的溶液中:Al3+、Fe2+、Cl﹣、NO ![]() 、S2﹣
、S2﹣
②使pH=11的溶液中:Na+、NO ![]() 、SO
、SO ![]() 、AlO2﹣、S2﹣
、AlO2﹣、S2﹣
③由水电离出的c(H+)=10﹣12mol/L的溶液中:Na+、NO ![]() 、SO
、SO ![]() 、AlO2﹣、S2﹣
、AlO2﹣、S2﹣
④能使淀粉碘化钾试纸显蓝色的溶液:K+、SO ![]() 、SO
、SO ![]() 、S2﹣、OH﹣
、S2﹣、OH﹣
⑤使甲基橙变红的溶液中:Fe3+、NH4+、Cl﹣、K+、SO42﹣ .
A.③④
B.②④
C.②⑤
D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某液态卤代烃RX(R是烷基,X是某种卤素原子)的密度是a g/cm3。该RX在稀碱溶液中可以发生水解反应生成有机物ROH(ROH能与水互溶)和HX。为了测定RX的相对分子质量,进行了如下实验操作:
①准确量取该卤代烃bmL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀HNO3溶液酸化,滴加过量AgNO3溶液,得到白色沉淀。
④过滤、洗涤、干燥后称重,得到cg固体。
回答下列问题:
(1)步骤④中,洗涤的目的是为了除去沉淀上吸附的___________离子。
(2)该卤代烃中所含卤素的名称是____________,判断的依据是_________________。
(3)该卤代烃的相对分子质量是______________________(列出算式)。
(4)如果在步骤②中,加HNO3的量不足,没有将溶液酸化,则步骤④中测得的c____(填写下列选项代码)。
A.偏大 B.偏小 C.不变 D.无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应在体积为2升的密闭容器中进行反应(A,B,C均为气体),在不同反应时间各物质的量的变化情况如图所示.则: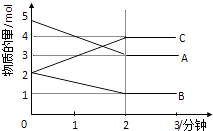
(1)该反应的化学方程为
(2)反应开始至2分钟,A的平均反应速率为
(3)反应开始至2分钟,A的转化率为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com