
 ���ᡢ���ᡢ̼��ȶ�����Ҫ��̼�Ļ������֪������Ϣ��
���ᡢ���ᡢ̼��ȶ�����Ҫ��̼�Ļ������֪������Ϣ��| ����Ļ�ѧʽ | CH3COOH | HCN | H2CO3 |
| ���볣�� | Ka=l.8��l0-5 | Ka=4.9��10-10 | Kal=4.3��10-7 Ka2=5.6��10-11 |
���� ��1��NaCN��ǿ�������Σ���Һˮ��ʼ��ԣ�
��2��25��ʱ�����CH3COOH��CH3COONa�Ļ����Һ��pH=6���ڷ�ʽ$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$�ķ��Ӻͷ�ĸͬ���������ӵ�Ũ�ȣ���$\frac{c��{H}^{+}��}{{K}_{a}}$��
��3������һŨ�ȵ�NaHCO3��Һ�У����������غ㣺c��OH-��+c��CO32-��=c��H+��+c��H2CO3�����ɴ˷������
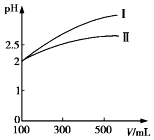
��4��CH3COOH�ĵ��볣��Ka=l.8��l0-5mol•L-1��HCN�ĵ��볣��Ka=4.9��10-10�����߶�������˵���������Դ������ᣬ��Խ����Ӧ�ε�ˮ��̶�Խ����Һ����Խ��
��5��Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L���������Ϻ���Һ��c��CO32-��=1��10-4mol/L������Ksp=c��CO32-��•c��Ca2+���������ʱ�����Һ��c��Ca2+����ԭ��ҺCaCl2��Һ����СŨ��Ϊ�����Һ��c��Ca2+����2����
��� �⣺��l��NaCN��ǿ�������Σ���Һˮ��ʼ��ԣ�ˮ��ķ���ʽΪ��CN-+H2O?HCN+OH-���ʴ�Ϊ��CN-+H2O?HCN+OH-��
��2��25��ʱ�����CH3COOH��CH3COONa�Ļ����Һ��pH=6���ڷ�ʽ$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$�ķ��Ӻͷ�ĸͬ���������ӵ�Ũ�ȣ���$\frac{c��{H}^{+}��}{{K}_{a}}$=$\frac{1{0}^{-6}}{l.8��l{0}^{-5}}$=$\frac{1}{18}$���ʴ�Ϊ��$\frac{1}{18}$��
��3������һŨ�ȵ�NaHCO3��Һ�У����������غ㣺c��OH-��+c��CO32-��=c��H+��+c��H2CO3�������� c��OH-��-c��H+��=c��H2CO3��-c��CO32-�����ʴ�Ϊ��=��
��4��CH3COOH�ĵ��볣��Ka=l.8��l0-5mol•L-1��HCN�ĵ��볣��Ka=4.9��10-10�����߶�������˵���������Դ������ᣬϡ����ͬ������ϡ����ͬ����������������ҺPH�仯С����HCN��ҺPH�仯С��IΪ����仯���ߣ��ʴ�Ϊ��I��
��5��Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L���������Ϻ���Һ��c��CO32-��=$\frac{1}{2}$��2��10-4mol/L=1��10-4mol/L������Ksp=c��CO32-��•c��Ca2+��=2.8��10-9��֪��c��Ca2+��=$\frac{2.8��1{0}^{-9}}{1��1{0}^{-4}}$mol/L=2.8��10-5mol/L��ԭ��ҺCaCl2��Һ����СŨ��Ϊ�����Һ��c��Ca2+����2������ԭ��ҺCaCl2��Һ����СŨ��Ϊ2��2.8��10-5mol/L=5.6��10-5mol/L��
�ʴ�Ϊ��5.6��l0-5mol/L��
���� ���⿼���ε�ˮ�⡢���볣����Ӧ�á������غ��Ӧ�ú��ܶȻ����йؼ��㣬���ؿ���ѧ���ķ����������������Ѷ��еȣ�ע���ܶȻ�����ʱ�����Ի�Ϻ���Һ��Ũ�ȷ����仯��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2 | B�� | NaHSO4 | C�� | HCl | D�� | KAl ��SO4��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -OH��  ���Ԫ����ͬ�����еĵ�����Ҳ��ͬ ���Ԫ����ͬ�����еĵ�����Ҳ��ͬ | |
| B�� | ��ϵͳ�������������� ��������2��3��4-����-2-�һ����� ��������2��3��4-����-2-�һ����� | |
| C�� | ������ӵ����ģ��ʾ��ͼ�� | |
| D�� | ��Ȳ�����ʽ��CH��CH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�����ͭ���ս�ճ�����մɶ��漰��ѧ�仯 | |
| B�� | �й��Ŵ�����������Һ���������ͭ�������ͭ�� | |
| C�� | ʳ�Ρ����ᡢ��ˮ�����ᱵ���ǵ���� | |
| D�� | ��������������ɢϵ�ı��������Ƿ�ɢ����ֱ����lnm〜l00nm֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuO | B�� | Cu20 | C�� | Cu | D�� | Cu��OH��2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����ͼ��ʾ������ʵ��װ���У���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.01mol���ӣ����������ε�ˮ�����Һ����ı仯����������������ȷ���ǣ�������
����ͼ��ʾ������ʵ��װ���У���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.01mol���ӣ����������ε�ˮ�����Һ����ı仯����������������ȷ���ǣ�������| A�� | �ұߵ缫���������ʵ���������=�� | |
| B�� | �����ϲ��������������٣��� | |
| C�� | ��Һ��pH�仯�������ڲ��� | |
| D�� | �缫��Ӧʽ����������2H2O-4e-=4H++O2�����и���2H+-2e-=H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ����������ӳ���KSCN��Һ��������Χ�����Ų�ʽΪ3d104s1����Ԫ�����ڱ��е�λ��Ϊ�������ڢ�B�壮
����������ӳ���KSCN��Һ��������Χ�����Ų�ʽΪ3d104s1����Ԫ�����ڱ��е�λ��Ϊ�������ڢ�B�壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl | B�� | Ba��OH��2 | C�� | CO2 | D�� | NH3•H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com