
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | FeCl3溶液滴在淀粉碘化钾试纸上,试纸变蓝:2Fe3++2I-═2Fe2++I2 | |
| C. | 铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 氯气溶于水:Cl2+H2O?H++Cl-+HClO |
分析 A.反应生成NaOH和氢气;
B.反应生成碘化亚铁、碘;
C.铁溶于稀硝酸,溶液变黄,生成硝酸铁;
D.反应生成盐酸和HClO,只有HCl完全电离.
解答 解:A.Na放入水中,产生气体的离子反应为2Na+2H2O═2Na++2OH-+H2↑,遵循电子、电荷守恒,故A正确;
B.FeCl3溶液滴在淀粉碘化钾试纸上,试纸变蓝的离子反应为2Fe3++2I-═2Fe2++I2,遵循电子、电荷守恒,故B正确;
C.铁溶于稀硝酸,溶液变黄的离子反应为Fe+4H++NO3-═Fe3++NO↑+2H2O,故C错误;
D.氯气溶于水的离子反应为Cl2+H2O?H++Cl-+HClO,故D正确;
故选C.
点评 本题考查离子方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒的判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A. | 该反应的化学方程式是:H2(g)+CO2(g)?CO(g)+H2O(g) | |
| B. | 上述反应的正反应是吸热反应 | |
| C. | 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,如果此时测得CO2为0.5 mol,则该反应达到平衡状态 | |
| D. | 某温度下,如果平衡常数符合下列关系式:$\frac{c(C{O}_{2})}{3c(CO)}$=$\frac{c({H}_{2}O)}{5c({H}_{2})}$,则此时温度700℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:戊烷>2-甲基丁烷>乙二醇 | |
| B. | 密度:硝基苯>H2O>汽油 | |
| C. | 等质量的物质燃烧耗O2量:乙烯>乙炔>甲烷 | |
| D. | 等物质的量物质燃烧耗O2量:丙烷>环丙烷>2-丙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
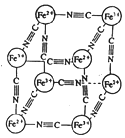 分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )
分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )| A. | 该晶体中含有共价键,是离子晶体 | |
| B. | M 离子位于晶胞面心,呈+2 价 | |
| C. | M 离子位于晶胞体心,呈+1 价,且 M+空缺率为 50%(体心中没有 M+占总体心的百分比) | |
| D. | 晶体的化学式可表示为 MFe2(CN)6,且 M 为+1 价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2完全转化为NH3时,即可视为达到化学平衡状态 | |
| B. | 达到化学平衡时,容器内压强和气体密度都不再变化 | |
| C. | 达到化学平衡时,反应则停止进行 | |
| D. | 达到化学平衡时,3ν(逆NH3)=2ν(正H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{20}^{40}$Ca 和${\;}_{18}^{40}$Ar | B. | D和T | ||
| C. | H2 O和H2 O2 | D. | O3 和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 异戊烯醇用于苯氯菊酯杀虫剂以及其他精细化学品的合成,是生产医药或农药的重要原
异戊烯醇用于苯氯菊酯杀虫剂以及其他精细化学品的合成,是生产医药或农药的重要原| A. | 分子式为C5H10O | |
| B. | 与氢气发生加成反应后生成物名称为2-甲基-丁醇 | |
| C. | 可使酸性KMnO4溶液褪色 | |
| D. | 与 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.下列说法不正确的是( )
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.下列说法不正确的是( )| A. | 该反应的化学方程式为3X+Y?2Z | |
| B. | 容器内混合气体的平均摩尔质量保持不变表明该反应一定达到平衡状态 | |
| C. | 平衡时,体系的压强是开始时的1.8倍 | |
| D. | 平衡时,Y的体积分数为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,c(NH4+)相同的溶液中,溶质的物质的量浓度:c(NH3•H2O)>c(CH3COONH4)>c(NH4Cl)>c(NH4HSO4) | |
| B. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量盐酸大于醋酸 | |
| D. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com