
| A. | 产品中有被蒸馏出的H2SO4 | B. | 有部分未反应的乙醇被蒸馏出来 | ||
| C. | 有部分未反应的乙酸被蒸馏出来 | D. | 有部分乙醇跟浓硫酸作用生成CO2 |
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4和CH3(CH2)15CH3 | B. | CH3(CH2)3CH3和CH(CH3)3 | ||
| C. | C2H4和CH3CH2CH3 | D. | C3H8和CH3(CH2)6CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年12月11日瑞典斯德哥尔摩诺贝尔奖颁奖典礼举行,授予中国女药学家屠呦呦、美国科学家威廉•坎贝尔和日本大村智诺贝尔医学奖,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图,下列说法错误的是( )
2015年12月11日瑞典斯德哥尔摩诺贝尔奖颁奖典礼举行,授予中国女药学家屠呦呦、美国科学家威廉•坎贝尔和日本大村智诺贝尔医学奖,以表彰他们在寄生虫疾病治疗方面取得的成就.屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图,下列说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | B. | 青蒿素是芳香族化合物 | ||
| C. | 青蒿素可以发生水解反应 | D. | 青蒿素含有过氧结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③正确 | B. | 只有①③正确 | C. | 只有④正确 | D. | 均不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
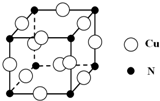 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: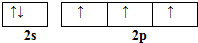 .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.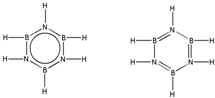 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com