
| A. | 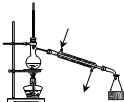 用于蒸馏石油 | B. | 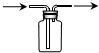 用于收集NO | ||
| C. | 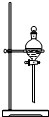 用于分离乙酸和乙酸乙酯混合物 | D. | 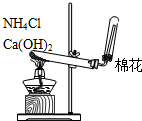 用于实验室制取NH3 |
分析 A.水的进出方向错误;
B.NO应用排水法收集;
C.乙酸和乙酸乙酯混溶,不能用分液的方法分离;
D.氯化铵和氢氧化钙反应生成氨气,氨气密度比空气小,可用向下排空法收集.
解答 解:A.蒸馏时,为充分冷凝,水应从下端进,上端出,故A错误;
B.NO易与氧气反应,应用排水法收集,用排水法收集时气体从短管进,故B错误;
C.乙酸和乙酸乙酯混溶,不能用分液的方法分离,可用蒸馏的方法分离,故C错误;
D.氯化铵和氢氧化钙反应生成氨气,氨气密度比空气小,可用向下排空法收集,可用于制备氨气,故D正确.
故选D.
点评 本题考查实验方案评价,为高考高频点,涉及物质的分离、气体的制备、收集等知识点,侧重实验操作和实验原理的考查,注意实验方案的操作性、可行性、评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1molSiO2含有2NA个Si-O键 | |
| B. | 1molNa2O2固体中含离子总数为3NA. | |
| C. | 标准状况下,22.4 L SO3所含分子数为NA. | |
| D. | 1L0.5mol/L的MgCl2溶液中,含有Mg2+个数为0.5NA. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12O且可与金属钠反应放出氢气的有机物有4种 | |
| B. | 甲苯分子中所有原子可能共面 | |
| C. | 苯、乙醇、油脂均不能使酸性KMnO4溶液褪色 | |
| D. | C3H2Cl6有四种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量守恒、电子守恒、电荷守恒 | B. | 电子守恒、质量守恒、电荷守恒 | ||
| C. | 电子守恒、电荷守恒、质量守恒 | D. | 电荷守恒、质量守恒、电子守恒 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C18H36O2 | B. | C19H36O2 | C. | C18H38O2 | D. | C19H38O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com