
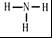 .
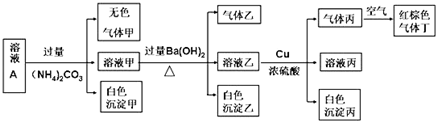
.分析 由溶液pH=1可知溶液为酸性溶液,溶液中存在大量氢离子,可以排除CO32-;
溶液A中加过量(NH4)2CO3,产生白色沉淀,白色沉淀只能为氢氧化铝,可以排除Fe2+、Fe3+,溶液含有一定有Al3+;
溶液乙加铜和浓硫酸能产生气体丙,丙在空气中变成红棕色,则丙为NO,原溶液中有NO3-,强酸性溶液中含有NO3-,则一定不存在具有还原性的离子为Fe2+、I-;
最后根据电荷守恒得原溶液中含有H+、NO3-、Al3+、SO42- Cl-五种离子,以此来解答.
解答 解:由溶液pH=1可知溶液为酸性溶液,溶液中存在大量氢离子,可以排除CO32-;
溶液A中加过量(NH4)2CO3,产生白色沉淀,白色沉淀只能为氢氧化铝,可以排除Fe2+、Fe3+,溶液含有一定有Al3+;
溶液乙加铜和浓硫酸能产生气体丙,丙在空气中变成红棕色,则丙为NO,原溶液中有NO3-,强酸性溶液中含有NO3-,则一定不存在具有还原性的离子:Fe2+、I-;
最后根据电荷守恒得原溶液中含有H+、NO3-、Al3+、SO42- Cl-五种离子.
(1)通过以上分析知,溶液A中一定不存在的阴离子有CO32-,故答案为:CO32-;
(2)沉淀甲是铝离子和碳酸根离子的双水解反应生成氢氧化铝沉淀和二氧化碳,生成沉淀乙是钡离子和碳酸根离子的反应,二者离子方程式分别为2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑、Ba2++CO32-=BaCO3↓,
故答案为:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑、Ba2++CO32-=BaCO3↓;
(3)铵根离子和氢氧根离子反应生成氨气,氨气分子中每个H原子和N原子之间共用一对电子,其结构式为 ,故答案为:
,故答案为: ;
;
(4)酸性条件下,铜和硝酸根离子发生氧化还原反应生成铜离子和NO,离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,根据转移电子守恒得V(NO)=$\frac{\frac{144g}{64g/mol}×(2-0)}{(5-2)}$×22.4L/mol=33.6L,
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;33.6L.
点评 本题考查常见离子的推断,为高频考点,把握实验流程中的反应、现象与结论等为解答的关键,侧重分析与推断、实验能力的考查,注意气体、沉淀的颜色及成分为推断的突破口,题目难度不大.


科目:高中化学 来源: 题型:推断题
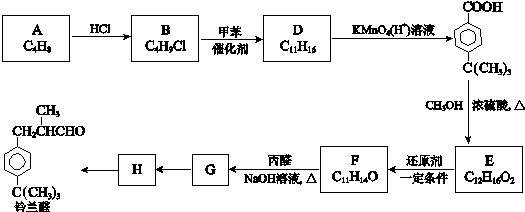
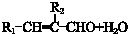
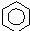 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$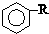 +HCl
+HCl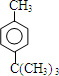 .
.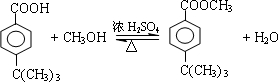 .
. .
. .
. .
.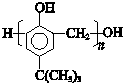 ,合成路线是(不需写化学方程式)
,合成路线是(不需写化学方程式)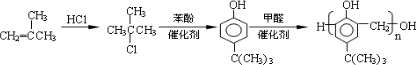 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NH4+、Cl-、H+、OH-的溶液中,离子浓度一定是c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | pH=6的醋酸与醋酸钠的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 将0.2 mol•L-1 CH3COOH溶液和0.1 mol•L-1 NaOH溶液等体积混合,则反应后的混合溶液中:2c(OH-)+c(CH3COO-)═2c(H+)+c(CH3COOH) | |
| D. | pH=8的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 、纯棉T恤是复合材料制品 | B. | 不锈钢领带别针是有机材料制品 | ||
| C. | 玻璃水杯是无机材料制品 | D. | 碳纤维增强网球拍是无机材料制品 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
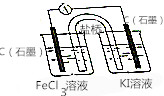 按如图所示装置(盐桥内含有KCl饱和溶液)线路连接后,可发现电流表指针明显偏转,说明发生了原电池反应,下列关于该电池的叙述正确的是( )
按如图所示装置(盐桥内含有KCl饱和溶液)线路连接后,可发现电流表指针明显偏转,说明发生了原电池反应,下列关于该电池的叙述正确的是( )| A. | 左侧石墨为电池的正极,电极反应:Fe3++e-═Fe2+ | |
| B. | 右侧烧杯中发生还原反应,电极反应:2I--2e-═I2 | |
| C. | 右侧烧杯内溶液颜色变浅 | |
| D. | 盐桥中的K+流向右侧烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁、铝在常温下都能被氧气氧化 | |
| B. | 将氯化铝和硫酸铝溶液蒸干灼烧后均得到氧化铝 | |
| C. | Na2O2与水反应,红热的铁与水蒸气反应均能生成碱 | |
| D. | Fe(OH)3不溶于水不能通过化合反应直接得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.
2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.根据掌握的信息分析,装箱区的危险化学品可能有钾、钠、氯酸钠、硝酸钾、烧碱,硫化碱、硅化钙、三氯乙烯、氯碘酸等.运抵区的危险化学品可能有环己胺、二甲基二硫、甲酸、硝酸铵、氰化钠、4,6-二硝基苯-邻仲丁基苯酚等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 金属铝溶于氢氧化钠溶液中:Al+2OH-═Al${O}_{2}^{-}$+H2↑ | |
| C. | 金属铝溶于盐酸中:2Al+6H+═2Al3++3H2↑ | |
| D. | Fe(OH)3跟盐酸反应:OH-+H+═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com