
| 100mL盐酸 | 100mL盐酸 | 100mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、盐酸物质的量浓度为1.5mol/L |
| B、15.7g混合物与盐酸反应后有剩余 |
| C、加入9.2 g混合物时消耗HCl 0.1mol |
| D、混合物中NaHCO3和KHCO3的质量比为1:1 |
| 3.36L |
| 2.24L |
| n |
| V |
| 3.36L |
| 2.24L |
| 3.36L |
| 22.4L/mol |
| 0.15mol |
| 0.1L |
| 2.24L |
| 22.4L/mol |
| 2.24L |
| 22.4L/mol |


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:高中化学 来源: 题型:
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中CO 的转化率与容器Ⅱ中CO2 的转化率之和等于1 |
| D、容器Ⅰ中CO 的物质的量比容器Ⅱ中的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3 |
| B、K2CO3和Na2CO3 |
| C、MgCO3和Na2CO3 |
| D、Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12% | B、78% |
| C、72% | D、13% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① |
| NaOH |
| ② |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气在阳极产生 |
| B、电解过程中Na+浓度不变 |
| C、水既不是氧化剂也不是还原剂 |
| D、反应过程是把化学能转化成电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:1 | B、1:2 |
| C、3:2 | D、2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯塑料的老化是由于发生了加成反应 |
| B、合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
C、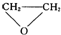 和CO2反应生成可降解聚合物[O-CHCH2-O-CO]n,该反应符合绿色化学的原则 和CO2反应生成可降解聚合物[O-CHCH2-O-CO]n,该反应符合绿色化学的原则 |
| D、煤经过气化和液化等物理变化可以转化为清洁燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com