
【题目】为测定某样品中氟元素的质量分数进行如下实验,利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(氢氟酸为低沸点酸,含量低,不考虑对玻璃仪器的腐蚀),用水蒸气蒸出,再通过滴定测量。实验装置如下图所示,加热装置省略。
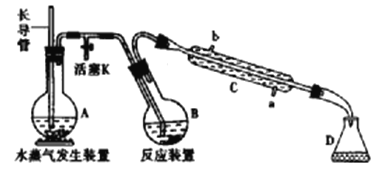
(1)A的名称是___________,长导管用于平衡压强,实验过程中其下端___________(填“能”或“不能”)在液面以上。
(2)仪器C是直形冷凝管,实验过程中,冷却水应从___________口出。(填“a”或“b")
(3)实验时,首先打开活塞K,待水沸腾时,关闭活塞K,开始蒸馏:若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即______________________。
(4)连接水蒸气发生装置和反应装置之间的玻璃管常裹以石棉绳,其作用是___________。
(5)B中加入一定体积高氯酸和1.00g氟化稀土矿样,D中盛有滴加酚酞的NaOH溶液。加热A、B,使A中产生的水蒸气进入B。
①下列物质不可代替高氯酸的是___________(填标号)
a.醋酸 b.硝酸 c.磷酸 d.硫酸
②D中主要反应的离子方程式为_________________________________。
(6)向馏出液中加入25.00mL0.100mol·L-1La(NO3)3溶液,得到LaF3沉淀,再用0.100 mol·L -1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1︰1络合),消耗EDTA标准溶液20.00mL,则氟化稀土样品中氟的质量分数为______________________。
【答案】圆底烧瓶 不能 b 打开活塞K 保温,避免水蒸气冷凝 ab HF+OH-=F-+H2O 2.85%
【解析】
A水蒸气发生装置,长导管作用起到平衡压强的作用,防止烧瓶内压强过大,实验时,首先打开活塞K,目的是让烧瓶内压强和外界一致,待水沸腾时,关闭活塞K,开始蒸馏,若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即打开活塞K,和外界联通降低压强,B制取HF的装置,利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢,用水蒸气蒸出,冷凝到D装置,被氢氧化钠中和吸收,在采用滴定法定量测定氟元素的质量分数。
(1)A的名称是圆底烧瓶,长导管用于平衡压强,实验过程中其下端在液面以下;
答案:圆底烧瓶 不能
(2)实验过程中,直形冷凝管中的冷却水应从a进b出,这样可使冷却水充满外管,有利于带走热量;
答案:b。
(3) 从实验安全角度考虑,实验时,首先打开活塞K,目的是让烧瓶内压强和外界一致,待水沸腾时,关闭活塞K,开始蒸馏,若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即打开活塞K,和外界联通降低压强;
答案:打开活塞K
(4)连接水蒸气发生装置和反应装置之间的玻璃管常裹以石棉绳,石棉绳的隔热效果比较好,主要起到保温防止水蒸气冷凝的作用;
答案:保温,避免水蒸气冷凝。
(5)①根据题干知识可知反应原理为高沸点酸(难挥发性酸)制取低沸点酸(易挥发性酸),醋酸和硝酸易挥发,不可代替高氯酸;
答案:ab
②D中是氢氧化钠与HF发生酸碱中和生成盐和水,离子方程式为HF+OH-=F-+H2O;
答案:HF+OH-=F-+H2O。
(6)关系式法计算:设F-的物质的量为x
3F-~LaF3~ La3+ EDTA ~ La3+
3mol 1mol 1mol 1mol
x x/3 0.1mol/L×20.00×10-3L 0.1mol/L×20.00×10-3L
![]() +0.1mol/L×20.00×10-3L=0.100mol/L×25.00×10-3L
+0.1mol/L×20.00×10-3L=0.100mol/L×25.00×10-3L
得x=1.5×10-3mol=0.0015mol
氟化稀土样品中氟的质量分数为:![]() ×100%=2.85%
×100%=2.85%
答案:2.85%


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的简化电子排布式为________。
(2)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含____molσ键,与CO互为等电子体的离子是_____(填化学式,写一种)。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3),钛酸亚铁与浓硫酸反应生成TiSO4,SO42—中S原子的杂化方式为____,用价层电子对互斥理论解释SO32—的键角比SO42—键角小的原因___________________________________________________。
(4)氮化铁晶体的晶胞结构如图所示。该晶体中铁、氮的微粒个数之比为____。

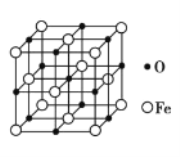
(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为____;Fe2+与O2—的最短核间距为____pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物a( )、b(
)、b(![]() -CH3)、c(
-CH3)、c(![]() )的说法正确的是
)的说法正确的是
A. a、b互为同分异构体 B. b、c均属于芳香化合物
C. c分子中所有碳原子共平面 D. a、b、c均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种化学性质活泼的气体。
(1)新制备的氯水呈_____色,说明氯水中有_____分子存在。向氯水中滴入几滴AgNO3溶液,现象是________,说明氯水中有_________存在,该反应的化学方程式_______________。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是____________。

(3)为防止氯气污染空气,可用______溶液吸收多余的氯气,该反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素X、Y、Z、W、R的原子序数依次增大,且它们的原子序数均不超过20。已知X原子最外层电子数是其最内层电子数的2倍,Y的最高正价与最低负价代数和为2,Z的周期数等于其族序数,W的最外层电子数与X的核外电子数相等,R的最外层电子数等于W和X的最外层电子数之差。下列说法正确的是
A.原子半径的大小顺序:r(W)>r(Z)>r(X)
B.最高价氧化物对应水化物的酸性:X>Y
C.常温下Z的单质与Y的最高价含氧酸浓溶液不发生反应
D.最高价氧化物对应水化物的碱性:Z<R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钪(Sc)是一种典型的稀散元素,具有重要的工业利用价值,从钛尾矿( mSc2O3·nTiO2·xFeO·ySiO2)中提取Sc2O3的流程如下:

(1)“焙烧”时,为提高焙烧效率,下列措施中无效的是___________(填标号)
a.不断搅拌 b.进一步粉碎固体颗粒 c.增大压强 d.适当升高温度
(2)“酸浸”时,需在80℃条件下进行,则适宜的加热方式为______________________。
(3)“萃取”时,使用伯胺N1923的煤油溶液作为萃取液,萃取率α受振荡时间和萃取剂浓度的影响,椴据下表1和表2数据,萃取时适宜的振荡时间和萃取剂浓度分别为___________min、___________%。

(4)“酸洗”后滤液中存在的金属阳离子有Na+、Sc3+、Ti4+、Fe2+,且浓度均小于0.100mol·L-1,“反萃取”时,加氢氧化钠溶液调节溶液pH=__________时,可使Sc3+沉淀完全(当离子浓度减小至10-5 mol·L-1时,可认为沉淀完全),从滤渣Ⅲ中可以回收的金属元素名称为__________。(已知;lg2=0.3,1g5=0.7;室温下,Ti4+完全沉淀的pH为1.05,Ksp[Fe(OH)2]=4.0×10-17,Ksp[Sc(OH)3]=1.25×10-33)
(5)草酸钪[Sc2(C2O4)3]在空气中“灼烧”的化学方程式为______________________。
(6)若从1吨该钛尾矿中提取得到110.4gSc2O3,则该矿中含钪的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、Z-、W2四种离子均具有相同的电子层结构
、Z-、W2四种离子均具有相同的电子层结构![]() 下列关于X、Y、Z、W四种元素的描述,不正确的是
下列关于X、Y、Z、W四种元素的描述,不正确的是![]()
![]()
A.原子序数:Y>X>Z>WB.离子半径:X+>Y2+>Z->W2-
C.原子最外层电子数:Z>W>Y>XD.还原性:X>Y>W2->Z-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。

I.用图甲所示装置进行第一组实验时:
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_____ (填字母)。
A石墨 B. 镁 C.银 D.铂
(2)实验过程中,SO42-____(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象是________________。
II.该小组同学用图乙所示装置进行第二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(FeO42-)在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
(3)电解过程中,X极处溶液的OH-浓度____(填“增大”“减小”或“不变)。
(4)电解过程中,Y极发生的电极反应为___________________,_________________。
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为____mL(均己折算为标准状况时气体体积)。
(6)K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电池反应总反应式为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设一个12C原子的质量为a g,一个16O原子的质量为b g,阿伏加德罗常数为NA,则12C16O2的相对分子质量与以下哪些数值相同
①a+2b ②(a+2b)NA ③![]() ④
④![]()
A.①③B.②③C.①④D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com