
硫单质及其化合物在工农业生产中有着重要的应用。
(1)已知25℃时:SO2(g)+2CO(g)=2CO2(g)+1/xSx(s)?? △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+3/xSx(s)?? △H=bkJ/mol。
则COS(g)生成CO(g)与Sx(s)反应的热化学方程式是????????????????????? 。
(2)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料。已知As2S3和HNO3有如下反应:As2S3+10H++ 10NO3?=2H3AsO4+3S+10NO2↑+ 2H2O,当生成H3AsO4的物质的量为0.6 mol反应中转移电子的数目为??????? ,
(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS?、S2?的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如下图所示(忽略滴加过程H2S气体的逸出)。
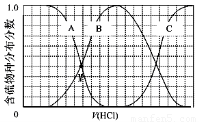
①B表示??? ??????????? 。
②滴加过程中,溶液中微粒浓度大小关系正确的是???? (填字母)。
a.c(Na+)= c(H2S)+c(HS?)+2c(S2?)
b.2c(Na+)=c(H2S)+c(HS?)+c(S2?)
c.c(Na+)=3[c(H2S)+c(HS?)+c(S2?)]
③NaHS溶液呈碱性,当滴加盐酸至M点时,溶液中各离子浓度由大到小的顺序为??????????????????????????????????????? 。
(4)工业上用硫碘开路循环联产氢气和硫酸的工艺流程如下图所示:
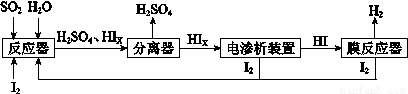
① 写出反应器中发生反应的化学方程式是?????????????????? 。
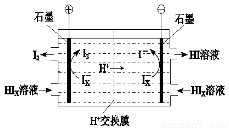
② 电渗析装置如图所示,写出阳极的电极反应式?????????????? 。该装置中发生的总反应的化学方程式是???????????????? 。
(1)xCOS(g)=xCO(g)+Sx(s)? △H=0.5x(b ? a)kJ/mol???
(2)3NA?? (2分 )
(3)①HS?(或NaHS) (2分) ②c (2分) ③c(Na+)> c(HS?)>c(S2?) >c(OH?)>c(H+)
(4) ①SO2 + x I2 + 2H2O = H2SO4 + 2HIX???? ②2Ix? -2e? = xI2? 2HIx=(x-1)I2 + 2HI
【解析】
试题分析:(1)①SO2(g)+2CO(g)=2CO2(g)+1/xSx(s)?? △H=akJ/mol
②2COS(g)+SO2(g)=2CO2(g)+3/xSx(s)?? △H=bkJ/mol。根据盖斯定律:②×1/2x—①×1/2x得COS(g)生成CO(g)与Sx(s)反应的热化学方程式是xCOS(g)=xCO(g)+Sx(s)? △H=0.5x(b ? a)kJ/mol;(2)根据反应As2S3+10H++ 10NO3?=2H3AsO4+3S+10NO2↑+ 2H2O知,当生成H3AsO4的物质的量为2 mol时转移的电子为10mol,则当生成H3AsO4的物质的量为0.6 mol反应中转移电子的数目为3NA ;(3)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量发生的反应依次为NaOH+HCl=NaCl+H2O,Na2S+HCl=NaHS+NaCl,NaHS+HCl=H2S+NaCl。①结合题给图像分析,B表示HS?(或NaHS);②根据物料守恒知,滴加过程中,溶液中微粒浓度大小关系为c(Na+)=3[c(H2S)+c(HS?)+c(S2?)],选c;③A表示Na2S,B为NaHS,当滴加盐酸至M点时,表示两者含量相等,溶液中c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],则c(Na+)>c(HS-),NaHS溶液呈碱性说明其水解大于电离,水解是微弱的所以c(HS-)>c(S2-),硫化钠为强碱弱酸盐,其溶液呈碱性,所以c(OH-)>c(H+),则c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+);(4)①由工艺流程图可知,SO2、I2、H2O反应生成H2SO4、HIX,反应方程式为:SO2+xI2+2H2O=H2SO4+2HIX;②由题给装置图可知,在阴极区Ix-转化为I-,在阳极区Ix-转化为I2,所以阳极区发生的反应为:2Ix--2e-=xI2,电解HIx生成I2、HI,反应方程式为:2HIx═(x-1)I2+2HI。
考点:考查盖斯定律、氧化还原反应、电解质溶液离子浓度大小比较和电解原理的应用。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
| c2(NH3) |
| c(N2)×c3(H2) |
| c2(NH3) |
| c(N2)×c3(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
| c2(NH3) |
| c3(H2)×c(N2) |
| c2(NH3) |
| c3(H2)×c(N2) |
| 7 |
| 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 时间(min) 浓度(mol/L) |
0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| x |
| 3 |
| x |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com