
(16分)(2012?广东)碘在科研与生活中有重要作用,某兴趣小组用0.50mol?L﹣1KI、0.2%淀粉溶液、0.20mol?L﹣1K2S2O8、0.10mol?L﹣1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
已知:S2O82﹣+2I﹣=2SO42﹣+I2(慢) I2+2S2O32﹣=2I﹣+S4O62﹣ (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32﹣与S2O82﹣初始的物质的量需满足的关系为:n(S2O32﹣):n(S2O82﹣) .
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验 序号 | 体积V/ml | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中Vx= ml,理由是 .
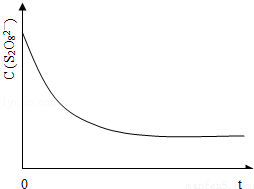
(3)已知某条件下,浓度c(S2O82﹣)~反应时间t的变化曲线如图13,若保持其它条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82﹣)~反应时间t的变化曲线示意图(进行相应的标注).
(4)碘也可用作心脏起捕器电源﹣锂碘电池的材料,该电池反应为:2Li(s)+I2 (s)=2LiI(s)△H
已知:4Li(s)+O2 (g)=2Li2O(s)△H1
4LiI(s)+O2 (g)=2I2 (s)+2Li2O(s)△H2
则电池反应的△H= ;碘电极作为该电池的 极.
(1)Na2S2O3;<2(2)2;理由是保证其他条件不变,只改变反应物K2S2O8浓度,从而才到达对照实验目的(3)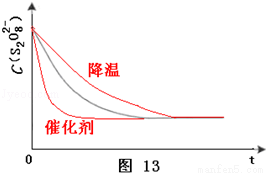 (4)
(4)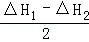 ;正极
;正极
【解析】(1)根据KI、Na2S2O3与淀粉的反应原理解答,注意反应过程的快慢问题;
(2)根据实验目的及表格数据分析,从而确定Vx的大小及理由,注意探究物质的量浓度对反应速率影响时,其它条件应相同;
(3)降低温度,化学反应速率减小,则到达平衡时间延长;加入催化剂,增大反应速率,则缩短反应到达平衡时间;
(4)将第一个方程式与第二个方程式相减再除以2,焓变进行相应改变,正极上得电子发生还原反应.
【解析】
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,先发生S2O82﹣+2I﹣═2SO42﹣+I2(慢),后发生I2+2S2O32﹣═S4O62﹣+2I﹣ (快),当S2O32﹣耗尽后,碘才能与淀粉作用显示蓝色,根据I2+2S2O32﹣═S4O62﹣+2I﹣ (快)方程式知,I2与S2O32﹣的物质的量的关系为1:2,即1mol碘需2molS2O32﹣,根据方程式S2O82﹣+2I﹣═2SO42﹣+I2知,生成1mol碘需为1molS2O82﹣,即n(S2O32﹣):n(S2O82﹣)=2:1,为确保能观察到蓝色,碘需有剩余,即n(S2O32﹣):n(S2O82﹣)<2:1,
故答案为:Na2S2O3;<2;
(2)对照实验1和2发现,实验2取的0.20mol?L﹣1K2S2O8溶液的体积9mL,比实验1少了1mL,说明取的K2S2O8物质的量少,加水1mL,保证了溶液的体积不变,所以在其它条件不变的情况下,探究的是该反应速率与K2S2O8浓度的关系,同样原理对照实验1和3,为保证溶液的体积相同,须加2mL水,
故答案为:2;理由是保证其他条件不变,只改变反应物K2S2O8浓度,从而才到达对照实验目的;
(3)保持其它条件不变,降低温度,反应速率降低,到达液颜色将由无色变成为蓝色的时间变长,而使用催化剂,能加快化学反应速率,所以到达液颜色将由无色变成为蓝色的时间变短,故答案为:
 ;
;
(4)①4Li(s)+O2 (g)=2Li2O(s)△H1
②4LiI(s)+O2 (g)=2I2 (s)+2Li2O(s)△H2
将方程式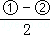 得2Li(s)+I2 (s)=2LiI(s),△H=
得2Li(s)+I2 (s)=2LiI(s),△H=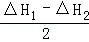 ,该反应中碘得电子发生还原反应,所以碘是在正极上发生反应,故答案为:
,该反应中碘得电子发生还原反应,所以碘是在正极上发生反应,故答案为: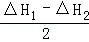 ;正极.
;正极.


 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源:2013-20147山东省乳山市下学期期中考试高二化学试卷(解析版) 题型:选择题
某有机物的化学式为C5H10O,能发生银镜反应和加成反应。若将它与H2加成,所得产物结构简式可能是
A.(CH 3)3COH B.(CH3CH2)2 CHOH
3)3COH B.(CH3CH2)2 CHOH
C.CH3(CH2)3CH2OH D.CH3CH2C(CH3)2OH
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(海南卷解析版) 题型:选择题
下列各组中,每种电解质溶液电解时只生成氢气和氧气的是
A.HCl、CuCl2、Ba(OH)2 B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2 D.NaBr、H2SO4、Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(新课标解析版) 题型:实验题
(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
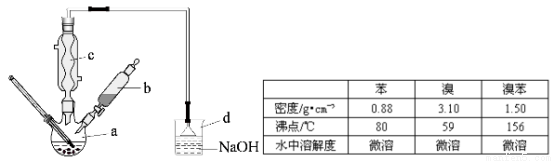
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(新课标解析版) 题型:选择题
NA表示阿伏伽德罗常数的值,下列叙述中不正确的是
A.分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(广东卷解析版) 题型:选择题
(4分)(2012?广东)设nA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温下,4g CH4含nA个C﹣H共价键
B.1 mol Fe与足量稀HNO3反应,转移个2nA个电子
C.1L 0.1 mol/L NaHCO3溶液中含有0.1nA个HCO3﹣
D.常温常压下,22.4L的NO2和CO2混合气体含有2nA个O原子
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(山东卷解析版) 题型:填空题
(12分)(2012?山东)石油和煤炭加工过程涉及多种技术和设备.
(1)石油分馏时,在不断向 (填工业设备名称)内投放原料的同时获得产品,该过程为 操作过程.
(2)石油裂化分为热裂化、 和加氢裂化,裂化的目的是提高 的产量.
(3)煤的洗选是为了降低原煤中灰分和 的含量.煤的流化床燃烧是指空气从底部吹向煤炭颗粒,并使全部煤炭颗粒 进行燃烧的过程.
(4)煤的直接液化是煤与适当溶剂混合后在高温和 存在下与 作用生成液体燃料的过程.
查看答案和解析>>
科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(大纲全国解析版) 题型:选择题
(2014?长宁区一模)①②③④甲种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是( )
A.①③②④ B.①③④② C.③④②① D.③①②④
查看答案和解析>>
科目:高中化学 来源:2012-2013陕西省富平县高一下学期期末考试化学试卷(解析版) 题型:选择题
一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是
| 正极 | 负极 | 电解质溶液 |
A | Zn | Cu | CuCl2 |
B | Zn | Cu | ZnCl2 |
C | Cu | Zn | CuSO4 |
D | Cu | Zn | ZnSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com