
 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:阅读理解
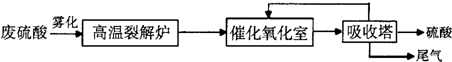
| 500-850℃ |
| 雾化后废硫酸液滴直径 | 废硫酸完全裂解所需时间 | |
| 普通雾化器 | 800-1200/μm | 10s以上 |
| 旋转式雾化器 | 600-850 μm | 8-10s |
| 压缩风雾化器 | 400-650 μm | 6-7s |
| 超声波雾化器 | 100-300μm | 3.5-5s |
查看答案和解析>>
科目:高中化学 来源: 题型:
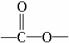
据此请完成下列问题:
(1)聚肉桂酸乙烯酯可水解为两种分子,一种不含苯环的名称为________;另一种含苯环的名称为肉桂酸,其结构简式为____________,分子式为____________。
(2)聚肉桂酸乙烯酯在光照下的二聚属________反应(填反应类型)。
(3)乙炔与肉桂酸在催化剂的作用下发生某种反应可获得聚肉桂酸乙烯酯的单体,写出该反应的化学方程?式(有机物用结构简式表示):_______________________________;该反应属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(A).【物质结构与性质】
下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| A | |||||||||||||||||
| B | C | ||||||||||||||||
| D | E | ||||||||||||||||
试回答下列问题:
(1)请写出元素D的基态原子电子排布式 ;
(2)D、E两元素的部分电离能数据列于下表:
| 元 素 | D | E | |
| 电离能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态D2+再失去一个电子比气态E2+再失去一个电子难。对此,你的解释是 ;
(3)A的氢化物的中心原子的杂化形式为 ;C在空气中燃烧产物的分子构型为 ,与其互为等电子体的单质的分子式为 。
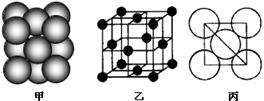 (4)B单质晶体中原子的堆积方式如右图甲所示,其晶胞特征如右图乙所示,原子之间相互位置关系的平面图如右图丙所示。晶胞中B原子的配位数为 ,一个晶胞中B原子的数目为 。
(4)B单质晶体中原子的堆积方式如右图甲所示,其晶胞特征如右图乙所示,原子之间相互位置关系的平面图如右图丙所示。晶胞中B原子的配位数为 ,一个晶胞中B原子的数目为 。
(B).【实验化学】
牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图,。

请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是 ,所需要的主要玻璃仪器有 。
(2)在②中用pH试纸测溶液的pH的操作方法是 。
(3)写出④中发生反应的化学方程
式: 。
(4)将⑤中放出的气体通入澄清的石灰水中时,未见沉淀出现,则可能的原因是 、
(任答两条)。
(5)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和 溶液的反应来进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示为实验室制取少量溴苯的装置,完成下列问题:

(1)烧瓶A中装的物质为____________________________________,发生反应的化学方程
式为________________________________。
(2)导管B的主要作用是______________________________________________。
(3)导管C处附近会出现白雾,其原因是
____________________________________________。
(4)反应后,向锥形瓶中滴加AgNO3溶液时,观察到的现象是_____________________,相应的离子方程式为______________________________________________。
(5)反应后,将烧瓶A中的液体倒入盛有冷水的烧杯中,烧杯底部有___________色的油状液体,带颜色的原因是________________________________,可用__________________的方法将颜色除去。
查看答案和解析>>
科目:高中化学 来源:2014届广东省师大附中高一下学期期考试化学试卷(解析版) 题型:填空题
(13分)氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)工业上利用分离空气的方法得到氮气。空气各主要成分的沸点如下:
|
N2 |
O2 |
Ar |
CO2 |
|
—196°C |
—183°C |
—186°C |
—78°C |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是 。
(2)雷雨时空气中的N2转化为NO,生成物NO是 色的气体, (填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应。NO2与水反应的化学方程式为 。
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气。
①制取氨气的化学方程为 ;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为 g。
(4)已知:4NH3+6NO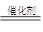 5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。
5N2+6 H2O 。化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能。
|

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。
①NH3与稀硫酸溶液反应的离子方程式为 ;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com