
【题目】下列图示与对应的叙述相符合的是

A. 图甲表示对某化学平衡体系改变温度后反应速率随时间的变化
B. 图乙表示反应物断键吸收的能量大于生成物成键放出的能量
C. 图丙表示0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化
D. 图丁表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况
科目:高中化学 来源: 题型:
【题目】下列事实不能用元素周期律解释的是( )
A. 热稳定性:Na2CO3>NaHCO3 B. 酸性:H2CO3>H2SiO3
C. 碱性:NaOH>LiOH D. 热稳定性:HF>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。某课外兴趣小组对X进行如下实验探究:

下列说法正确的是( )
A. 12.8g固体可能为Fe2O3 B. 混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
C. Fe2O3、Cu的物质的量之比为1:1 D. m>24.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为Na3AlF6 ,其中含有_______________________________等化学键。
(2)生成物中含有10个电子的分子是________(写分子式),该分子的空间构型_______,中心原子的杂化方式为___________________。
(3)反应物中所含元素电负性最大的元素为________(填元素符号),写出其原子最外层的电子排布图:_______________,它的氢化物的沸点比同主族其它氢化物的沸点高,原因是:_______________________________。
(4)冰晶石由两种微粒构成,它的晶胞结构如图甲所示,小黑点“●”位于大立方体的顶点和面心,小圆圈“○”位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处小三角“”所代表的是__________(填“小黑点”或“小圆圈”),它代表的是______________(填微粒化学式)。
(5)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
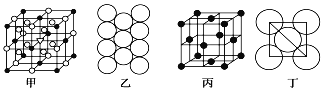
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目为___________个; Al晶体的密度为__________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类与化学式不相符的是
A.Na2O------碱性氧化物B.NaHCO3-------酸式盐
C.CH4-------有机物D.Na2CO3 ---------碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类文明的物质基础和先导,是直接推动社会发展的动力。
①现有下列材料:①钢化玻璃、②玻璃钢、③有机玻璃、④石英玻璃,其中与普通玻璃成分相同的是_______(填序号,下同),属于塑料的是______,属于复合材料的是_______,与光导纤维主要成分相同的是_______;生产普通玻璃的原料为__________(写化学式)。
②氧气和四氯化硅蒸气在旋转的高温炉中反应(发生置换反应),其产物之一可制得光导纤维,该反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液里大量共存的是
A.K+、Na+、OH-、Cl-B.Mg2+、Na+、SO42-、OH-
C.Cu2+、Ba2+、SO42-、Cl-D.H+、Ca2+、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前两年华北地区频繁出现的雾霾天气引起了人们的高度重视,化学反应原理可用于治理环境污染,请回答以下问题。
(1)一定条件下,可用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:2CO(g) + O2(g) = 2CO2(g) ΔH = 566 kJ·mol1
S(l) + O2(g) = SO2(g) ΔH = 296 kJ·mol1
则用CO处理燃煤烟气的热化学方程式是________________________。
②在一定温度下,向2 L 密闭容器中充入 2 mol CO、1 mol SO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K = _________________。
(2)SNCR─SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:

已知该方法中主要反应的热化学方程式:
4NH3(g) + 4NO(g) + O2(g) 4N2(g) + 6H2O(g) ΔH = 1646 kJ·mol1,在一定温度下的密闭恒压的容器中,能表示上述反应达到化学平衡状态的是__________________(填字母)。
a.4υ逆(N2) = υ正(O2)
b.混合气体的密度保持不变
c.c(N2):c(H2O):c(NH3)=4:6:4
d.单位时间内断裂4 mol N─H键的同时断裂4 mol N≡N键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
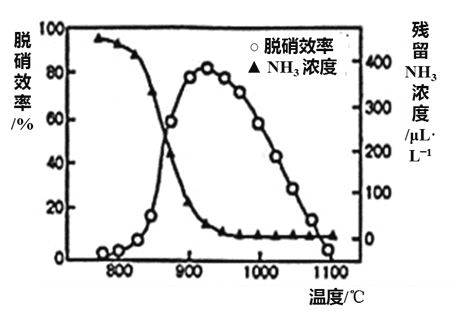
①SNCR技术脱硝的温度选择925 ℃的理由是___________________。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是____________________________________;但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是_____________________。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
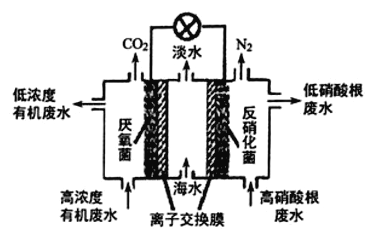
①中间室的Cl 移向_________(填“左室”或“右室”),处理后的含硝酸根废水的pH__________(填“增大”或“减小”)
②若图中有机废水中的有机物用C6H12O6表示,请写出左室发生反应的电极反应式:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com