
 某反应过程中体系的能量变化如图所示,下列说法错误的是( )
某反应过程中体系的能量变化如图所示,下列说法错误的是( )

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
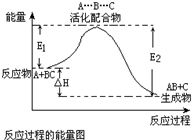
| A、反应过程可表示为A+BC-→[A…B…C]-→AB+C (反应物)(过渡态) (产物) | B、E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 | C、正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应 | D、此图中逆反应的热效应△H=E1-E2,为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程中体系的能量变化如图所示,下列说法错误的是
A、反应过程可表示为 A+BC—→[A…B…C] —→AB+C
(反应物)(过渡态) (产物)
B、此图中逆反应的热效应△H=E1—E2,为吸热反应
C、正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D、E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期第一次月考化学试卷(解析版) 题型:选择题
某反应过程中体系的能量变化如图所示,下列说法错误的是

A、反应过程可表示为 A+BC—→[A…B…C] —→AB+C
(反应物)(过渡态) (产物)
B、此图中逆反应的热效应△H=E1—E2,为吸热反应
C、正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D、E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
查看答案和解析>>
科目:高中化学 来源:2013届福建省高二上学期期中联考化学试卷 题型:选择题
某反应过程中体系的能量变化如图所示,下列说法错误的是 ( )

A. 反应过程可表示为A+BC—→[A…B…C] —→AB+C(反应物)(过渡态)(产物)
B. E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1—E2,为吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com