
 SOCl2��һ����Ҫ�Ļ�ѧ�Լ����������л��ϳɵ��Ȼ���������SOCl2��ˮ���ҷ�Ӧ�����ʣ������ڽ���ˮ���Ȼ������ˮ����SOCl2��������ص��������ϣ�
SOCl2��һ����Ҫ�Ļ�ѧ�Լ����������л��ϳɵ��Ȼ���������SOCl2��ˮ���ҷ�Ӧ�����ʣ������ڽ���ˮ���Ȼ������ˮ����SOCl2��������ص��������ϣ�| SO3 | SCl2 | SOCl2 | SO2 | |
| �۵� | 16.8�� | -122�� | -104.5�� | -75.5�� |
| �е� | 44.8�� | 59�� | 76�� | -10�� |
| ��ɫ | ��ɫ | ӣ�Һ�ɫ | ��ɫ | ��ɫ |
| ��ע | ���ȶ� | ���ȶ����е����Ϸֽ� |
���� ��1������Aװ���и������������Լ��������������ƽ��н�𣻸����Ʊ�SOCl2�ij��÷����ǣ�SO3+SCl2=SOCl2+SO2���Լ���Ӧ�����������ɫ������Ӧ���ʱ��������
��2��SOCl2��ˮ���ҷ�Ӧ��B����ʢҩƷ�Ǹ������װ��C���ȥβ�������������ü�Һ���գ�
��3������SOCl2�ķе����������¶ȣ�
��4��Liʧ����Ϊ������SOCl2Ϊ������
��5������﮵Ļ������Լ�SOCl2�����ʷ�����
��6��6.9g�����Ϊ1mol����ȫ��Ӧת�Ƶ���Ϊ1mol������W=UIt=UQ=nQ��Q=F��ת�Ƶ�������������=$\frac{����������}{�������}$���㣮
��� �⣺��1��Aװ����δ֪���Ƶ�������������������©�������в���������Ϊ��Һ©�����Ʊ�SOCl2�ij��÷����ǣ�SO3+SCl2=SOCl2+SO2��SO3��SO2����Ϊ��ɫ���壬��SCl2��Ϊӣ�Һ�ɫ��Һ�壬���Ե�������ƿ�з�Ӧ�����ӣ�Һ�ɫ��Ϊ��ɫ����ʱ��˵����Ӧ��ɣ�ֹͣ�μ�SO3��
�ʴ�Ϊ����Һ©����ӣ�Һ�ɫ��Ϊ��ɫ��
��2��SOCl2������ˮ���ҷ�Ӧ�����ʣ��÷�Ӧ�ĸ�����Ϊ��������Ϊ������Ⱦ����ü�Һ���գ�Ϊ��ֹβ������װ���е�ˮ����Aװ�ã�����Ũ������и��
�ʴ�Ϊ��Ũ����������ơ�����β����
��3��SOCl2�ķе�Ϊ76�棬���Է�Ӧ��A�л������������ռ����ϴ����IJ�Ʒ������������¶���76�棬
�ʴ�Ϊ��C��
��4��Liʧ����Ϊ������SOCl2Ϊ������������SOCl2�õ��ӷ�����ԭ��Ӧ�����ݷ�Ӧ����ʽ֪��SOCl2�õ�������LiCl��S��SO2���������ĵ缫����ʽΪ��2SOCl2+4Li++4e-=4LiCl+S+SO2��
�ʴ�Ϊ��2SOCl2+4Li++4e-=4LiCl+S+SO2��
��5��﮺�����ͬһ�����Ԫ�أ����ʾ��������ԣ��ƺͿ����е�������ˮ������Ӧ������﮺Ϳ����е�������ˮ����Ҳ�ܷ�Ӧ��SOCl2Ҳ����ˮ��Ӧ��������װ�õ�ر�������ˮ�������������½��У�
�ʴ�Ϊ����ǻ��ý���������H2O��O2��Ӧ��SOCl2Ҳ����ˮ��Ӧ��
��6��6.9g�����Ϊ1mol����ȫ��Ӧת�Ƶ���Ϊ1mol��W=UIt=UQ=nQ��Q=F��ת�Ƶ�������������=$\frac{����������}{�������}$=$\frac{F��n}{m��1{0}^{-3}��3.6��1{0}^{3}}$=$\frac{2.68��1{0}^{4}n}{m}$W•h•kg-1��
�ʴ�Ϊ��$\frac{2.68��1{0}^{4}n}{m}$��
���� ���⿼����SOCl2���Ʊ������ͻ�ѧ��Դ��֪ʶ����Ŀ�Ѷ��еȣ�ע���������е���Ϣ�Լ�ԭ��ص������жϼ��͵缫����ʽ����д�����������ڿ���ѧ���ķ��������ͼ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe������Cl2��ȼ������FeCl2 | |
| B�� | �����ʵ������ͱ��Ծ��ǻ�ѧ�仯 | |
| C�� | ��ѧ��Ӧ���ʱ��뷴Ӧ����������״̬�� | |
| D�� | ��a��b����;����ͭ�Ʊ���ͬ��������ͭ��;��a��b���ĵ�ͭһ���� ;��a��Cu$��_{��}^{O_{2}}$CuO$\stackrel{ϡ����}{��}$Cu��NO3��2��;��b��Cu$\stackrel{ϡ����}{��}$Cu��NO3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� | ��Ҫ�������� |
| A | �屽 | �� | �������ۺ��壬���� |
| B | �Ȼ��� | �Ȼ�� | ���� |
| C | ���������е�117.7�� | ���ѣ��е�34.5�� | ���� |
| D | �������� | ���� | ���뱥��̼������Һ����Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2H2��g��+O2��g���T2H2O��l����H1 2H2��g��+O2��g���T2H2O��g����H2 | |
| B�� | S��g��+O2��g���TSO2��g����H1 S��s��+O2��g���TSO2��g����H2 | |
| C�� | C��s��+$\frac{1}{2}$O2��g���TCO��g����H1 C��s��+O2��g���TCO2��g����H2 | |
| D�� | H2��g��+Cl2��g���T2HCl��g����H1$\frac{1}{2}$H2��g��+$\frac{1}{2}$Cl2��g���THCl��g����H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
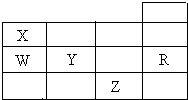 ���ΪԪ�����ڱ�ǰ�����ڵ�һ���֣�X��W��Y��R��Z�ֱ����Ԫ�ط��ţ�����RԪ�ص�ԭ��ÿ�����Ӳ㶼�ﵽ�ȶ��ṹ��������������ȷ���ǣ�������
���ΪԪ�����ڱ�ǰ�����ڵ�һ���֣�X��W��Y��R��Z�ֱ����Ԫ�ط��ţ�����RԪ�ص�ԭ��ÿ�����Ӳ㶼�ﵽ�ȶ��ṹ��������������ȷ���ǣ�������| A�� | XZ3��ƽ���������η��� | |
| B�� | ����X�γɵĻ�����Na3X��NaX3���Ǻ��й��ۼ������Ӿ��� | |
| C�� | W��YԪ�ص�����������Ӧ��ˮ��������ǰ�����ں��� | |
| D�� | X���⻯���W���⻯���ȶ������е�ǰ�߱Ⱥ��ߵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
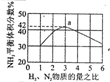 |  | 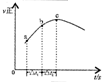 | 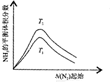 |
| ����ͼ��a�����ݼ���N2��ƽ�����������14.5% | ��ʾ��ͨ��ԭ�Ͽ�ʼ�����¶Ȳ������ߣ�NH3���ʵ����仯������ʾ��ͼ | ����Ⱥ�������ͨ��N2��H2����t1=��t2ʱ��N2��ת���ʣ�a-b�δ���b-c�� | ͼ��T2��T1 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
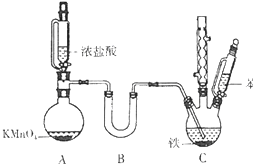 �ȱ�����Ҫ���л�����ԭ�ϣ�ʵ�����Ʊ��ȱ��ķ�Ӧԭ����ʵ��װ����ͼ��ʾ������װ������ȥ����
�ȱ�����Ҫ���л�����ԭ�ϣ�ʵ�����Ʊ��ȱ��ķ�Ӧԭ����ʵ��װ����ͼ��ʾ������װ������ȥ����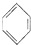 +Cl2$\stackrel{FeCl_{3}}{��}$
+Cl2$\stackrel{FeCl_{3}}{��}$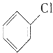 +HCl
+HCl| �е㣨�棩 | �ܶȣ�g•mL-1�� | �ܽ��� | |
| �� | 80.1 | 0.88 | ������ˮ |
| �ȱ� | 132.2 | 1.10 | ������ˮ���������л��ܼ� |
| �Զ��ȱ� | 173.4 | 1.46 | ������ˮ���������л��ܼ� |
| �ڶ��ȱ� | 180.4 | 1.30 | ������ˮ���������л��ܼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
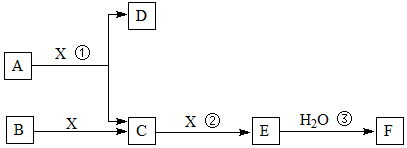
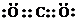 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com