
| A、白磷和红磷 |
| B、23Na和22Na |
| C、葡萄糖和蔗糖 |
| D、CH3CH(CH3)CH3和CH3CH2CH2CH3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、T℃时,测得某NaNO2溶液的pH=8,则溶液中c(Na+)-c(NO2-)=9.9×10-7mol?L-1 | ||||||||
| B、已知25℃时,有关弱电解质的电离平衡常数:HCN:Ka=4.9×10-10;H2CO3:Ka1=4.3×10-8,Ka2=5.6×10-11.则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2=2HCN+Na2CO3 | ||||||||
C、一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| ||||||||
| D、已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I-、ClO-、K+、H+ |
| B、Na+、Cu2+、Cl-、SO42- |
| C、H+、Ca2+、Cl-、CO32- |
| D、Na+ Cl- NO_- CO_2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Al3+、Cl-、SO42- |
| B、Cu2+、Cl-、NO3-、OH- |
| C、Ca2+、Na+、CO32-、NO3- |
| D、H+、SO42-、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(H+) |
| B、Na2CO3溶液中:c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+) |
| C、加入少量NaOH固体,水解平衡左移,溶液pH增大 |
| D、稀释该溶液,溶液中c(H+)和c(OH-)都减少,KW减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| B、CH3COOH溶液中加少量的CH3COONa固体,平衡正向移动 |
| C、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| D、常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:C(Na+)>C(SO42-)>C(NH4+)>C(OH-)=C(H+) |
| B、0.1mol?L-1pH为4的NaHB溶液中:C(HB-)>C(H2B)>C(B2-) |
| C、10mL 0.5mol?L-1 CH3COONa溶液与6mL 1mol?L-1盐酸混合:C(Cl-)>C(Na+)>C(CH3COO-)>C(H+)>C(OH-) |
| D、pH相等且处于相同温度下的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液C[(NH4)2SO4]<C[(NH4)2Fe(SO4)2]<C(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:
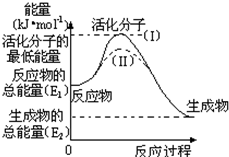 在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ?mol-1表示.请认真观察图,然后回答问题.
在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ?mol-1表示.请认真观察图,然后回答问题.| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com