B
分析:A.过氧化钠中的阴离子是过氧根离子;
B.O
3和O
2都是由氧原子构成,故氧原子的质量为3.2g,根据n=

计算氧原子的物质的量,再根据N=nN
A计算氧原子数目;
C.硫酸铝是强酸弱碱盐,铝离子易水解;
D.根据氧气和转移电子之间的关系式计算.
解答:A.7.8g Na
2O
2的物质的量是1mol,一个过氧化钠化学式中含有一个阴离子,所以7.8g Na
2O
2含有的阴离子数目为0.1N
A,故A错误;
B.3.2gO
3和O
2混合气体中氧原子的质量为3.2g,故n(O)=
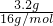
=0.2mol,含有的氧原子数为0.2mol×N
Amol
-1=0.2N
A,故B正确;
C.铝离子易水解,导致1L 0.1 mol/L的 Al
2(SO
4)
3溶液中,Al
3+的数目小于0.2 N
A,故C错误;
D.过氧化氢分解制得标准状况下1.12 L O
2,转移电子数目=
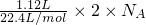
=0.1N
A,故D错误;
故选B.
点评:本题考查阿伏伽德罗常数,明确物质的构成、盐类的水解、电子转移即可分析解答,易错选项是A,注意过氧化钠中阴离子是过氧根离子而不是氧离子,为易错点.

 计算氧原子的物质的量,再根据N=nNA计算氧原子数目;
计算氧原子的物质的量,再根据N=nNA计算氧原子数目;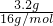 =0.2mol,含有的氧原子数为0.2mol×NAmol-1=0.2NA,故B正确;
=0.2mol,含有的氧原子数为0.2mol×NAmol-1=0.2NA,故B正确;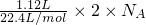 =0.1NA,故D错误;
=0.1NA,故D错误;

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案