
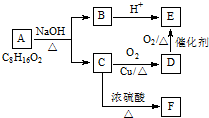
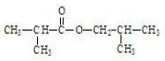 .F能使Br2的CCl4溶液褪色,则C在浓硫酸、加热条件下发生消去反应生成F为(CH3)2C=CH2,据此解答.
.F能使Br2的CCl4溶液褪色,则C在浓硫酸、加热条件下发生消去反应生成F为(CH3)2C=CH2,据此解答.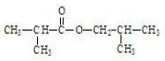 .F能使Br2的CCl4溶液褪色,则C在浓硫酸、加热条件下发生消去反应生成F为(CH3)2C=CH2,
.F能使Br2的CCl4溶液褪色,则C在浓硫酸、加热条件下发生消去反应生成F为(CH3)2C=CH2, ,反应方程式为n(CH3)2C=CH2
,反应方程式为n(CH3)2C=CH2| 催化剂 |
 ,故答案为:n(CH3)2C=CH2
,故答案为:n(CH3)2C=CH2| 催化剂 |
 ;
; ,
, ;
;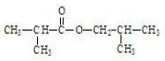 )小8,则其分子式可能为C8H8O2或C9H12O;
)小8,则其分子式可能为C8H8O2或C9H12O; 等;
等;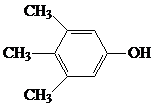 ,
, 等;
等;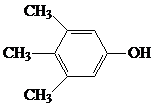 .
.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
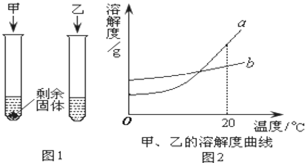 20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到
20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蓝色的淀粉溶液中通入足量SO2后成无色溶液:I2+SO2+2H2O=2I-+SO42-+4H+ |
| B、饱和Na2CO3溶液中通入CO2足量:2Na++CO32-+CO2+H2O=2NaHCO3↓ |
| C、钠投入CuSO4溶液中:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑ |
| D、向酸性KMnO4溶液中加入H2O2:2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
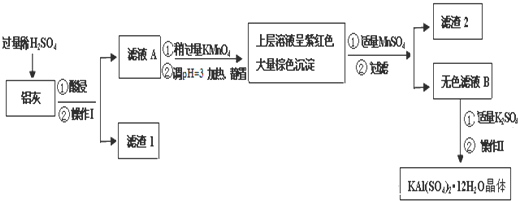
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定管出口部分开始有气泡,滴定后气泡消失 |
| B、锥形瓶用蒸馏水冲洗后随即使用 |
| C、当看到锥形瓶中溶液的颜色发生变化后随即停止了滴定 |
| D、滴定管在用蒸馏水洗净后,即装入标准的酸溶液进行滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Mg2+、Cl-、ClO- |
| B、NH3?H2O、SO32-、K+、Na+ |
| C、Fe2+、Na+、K+、NO3- |
| D、K+、Ca2+、Br-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子 |
| B、食用地沟油对人体的危害极大,原因主要是里面含有黄曲霉素和甘油三酯 |
| C、保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |
| D、地沟油分子中碳原子数过多,相对分子质量过大是地沟油不宜直接用作燃料油的原因之一 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com