
【题目】已知钠与氧气在不同条件下会发生不同的反应。
(1)将金属钠长时间放置于空气中可发生如下一系列变化,写出此变化中①③步转化的化学方程式:
Na![]() Na2O
Na2O![]() NaOH
NaOH![]() Na2CO3·10H2O→Na2CO3
Na2CO3·10H2O→Na2CO3
①___________;
③__________。
(2)将钠置于坩埚内,在空气中加热,可燃烧生成一种淡黄色物质。
①钠在空气中燃烧的化学方程式为___________。
②某学习小组通过实验研究Na2O2与水的反应。
操作 | 现象 |
向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生能使带火星木条复燃的气体,得到的无色溶液a |
向溶液a中滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
Na2O2与水反应的离子方程式是___________,甲同学认为过氧化钠中阴离子结合水中氢离子生成了H2O2,溶液a中的H2O2将酚酞氧化导致褪色。用实验证实H2O2的存在:取少量溶液a,加入试剂___________(填化学式),有气体产生。
【答案】4Na+O2=2Na2O 2NaOH+CO2+9H2O=Na2CO310H2O 2Na+O2![]() Na2O2 2Na2O2+2H2O=4Na++4OH-+O2↑ MnO2
Na2O2 2Na2O2+2H2O=4Na++4OH-+O2↑ MnO2
【解析】
(1)反应①是钠和氧气在常温下生成氧化钠;反应③是NaOH和CO2反应生成Na2CO310H2O;
(2)①钠在空气中燃烧生成过氧化钠;
②能使带火星木条复燃的气体是氧气,碱使酚酞变红,说明过氧化钠和水反应生成氢氧化钠和氧气;双氧水在MnO2的催化作用下发生分解反应生成氧气;
(1)反应①是钠和氧气在常温下生成氧化钠,反应方程式是4Na+O2=2Na2O;反应③是NaOH和CO2反应生成Na2CO310H2O,反应方程式是2NaOH+CO2+9H2O=Na2CO310H2O;
(2)①钠在空气中燃烧生成过氧化钠,反应方程式是2Na+O2![]() Na2O2;
Na2O2;
②过氧化钠和水反应生成氢氧化钠和氧气,反应的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑;双氧水在MnO2的催化作用下发生分解反应生成氧气,取少量溶液a,加入试剂MnO2,有气体产生,能证明H2O2的存在。


科目:高中化学 来源: 题型:
【题目】工业上常用NCl3制备消毒剂ClO2,利用如图装置电解氯化铵和盐酸的混合溶液可制备NCl3(已知NCl3的水溶液具有漂白性)。下列推断正确的是( )

A.石墨极为正极
B.铁极附近溶液的pH减小
C.每生成1 mol NCl3必转移3 mol电子
D.电解反应为NH4Cl+2HCl![]() NCl3+3H2↑
NCl3+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体粉末可能是硫酸铜(白色),硫酸铁(灰白色)或两者混合物,为探究其组成,取mg固体粉末溶于足量水配成溶液,该溶液最多可溶解ag铁粉。
(1)若固体为纯净硫酸铁粉末,则a=_____。(用含m的最简式表示);
(2)当a=m/6,恰好可以使得溶液中的金属阳离子只有一种,则固体粉宋中硫酸铜的物质的量为_____mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol Cl-、ClOx- (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是 ( )
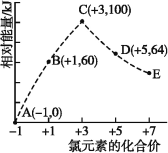
A.这些离子中结合H+能力最强的是A
B.A、B、C、D、E五种微粒中C最稳定
C.C→B+D的反应,反应物的总键能小于生成物的总键能
D.B→A+D反应的热化学方程式为3ClO-(aq)=ClO3- (aq)+2Cl-(aq) ΔH=+116 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用10mL的0.1mol·L-1BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.3∶1∶1B.3∶2∶2C.1∶2∶3D.1∶3∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
【资料查阅】

【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)D装置的作用_________________。
(2)装置D中发生的氧化还原反应的离子方程式是________________。
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是____________。
(4)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuO杂质,根据资料信息分析:则产生的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冶金工业、硝酸工业的废气废液中含氮化合物污染严重,必须处理达标后才能排放。
Ⅰ.用活性炭处理工厂尾气中的氮氧化物。
(1)已知:①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH1=a kJ·mol-1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΔH2=b kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH3=c kJ·mol-1
则反应C(s)+2NO(g) ![]() N2(g)+CO2(g)的ΔH=_____。
N2(g)+CO2(g)的ΔH=_____。
(2)在容积不变的密闭容器中,一定量的NO与足量的C发生反应:C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图1所示,下列说法正确的是______。
N2(g)+CO2(g) ΔH=Q kJ·mol-1,平衡时c(NO)与温度T的关系如图1所示,下列说法正确的是______。

A.其他条件不变,改变活性炭的用量,平衡一定不移动
B.该反应的Q>0,所以T1、T2、T3对应的平衡常数:K1<K2<K2
C.温度为T2时,若反应体系处于状态D,则此时v正>v逆
D.若状态B、C、D体系的压强分别为p(B)、p(C)、p(D),则p(D)=p(C)>p(B)
(3)已知某温度时,反应C(s)+2NO(g) ![]() N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图2中画出反应过程中c(NO)随时间t的变化曲线。_______
N2(g)+CO2(g)的平衡常数K=9/16,在该温度下的2 L密闭容器中投入足量的活性炭和2.0 mol NO发生反应,t1时刻达到平衡,请在图2中画出反应过程中c(NO)随时间t的变化曲线。_______
(4)工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:______________。
Ⅱ.用纳米铁粉或电解法处理废水中的硝酸盐。
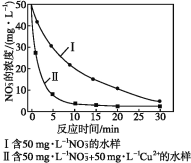
(5)纳米铁粉处理污水中NO3-的离子方程式为4Fe+ NO3-+10H+=4Fe2++NH4++3H2O。
实验证实,pH偏小将会导致NO3-的去除率下降,其原因是_______________。相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见图),产生该差异的可能原因是__。
(6)电解法处理水中硝酸盐的原理是以金属Pt作电极,用质子交换膜把溶液分为阴阳两极区,阴极区为含硝酸盐的工业废水,接通直流电源进行电解。请写出阴极的电极反应式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应N2O4(g) ![]() 2NO2(g)的焓变为ΔH。现将1 mol N2O4充入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
2NO2(g)的焓变为ΔH。现将1 mol N2O4充入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产、生活中有着重要作用。
(1)在T℃时,将0.6molH2和0.4molN2置于容积为2 L的密闭容器中(压强为mPa)发生反应:3H2+N2![]() 2NH3△H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为___mol·L-1·min-1。
2NH3△H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为___mol·L-1·min-1。

(2)仍在T℃时,将0.6molH2和0.4molN2置于一容积可变的密闭容 器中。
①下列各项能说明该反应已达到平衡状态的是______(填序号)。
a.容器内N2、H2、NH3的浓度之比为l:3:2
b.3v正(N2)=v逆(H2)
c.3v正(H2)=2v逆(NH3)
d.混合气体的密度保持不变
e.容器中气体的平均相对分子质量不随时间而变化
②该条件下达到平衡时NH3的体积分数与题(1)条件下NH3的体积分数相比________(填“变大”“变小”或“不变”)。
③达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改 变的条件可能是_________。

a.升高温度,同时加压
b.降低温度,同时减压
c.保持温度、压强不变,增大反应物浓度
d.保持温度、压强不变,减小生成物浓度
(3)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。 氨气能将氮氧化物还原为氮气和水,其反应机理为:
2NH3(g)+5NO2(g)=7NO(g)+3H2O(g)![]() H=-akJ·mol-1
H=-akJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)![]() H=-bkJ·mol-1
H=-bkJ·mol-1
则NH3直接将NO2还原为N2的热化学方程式为:______________。
若标准状况下NO与NO2混合气体40.32L被足量氨水完全吸收,产生标准状况下氮气42.56L。该混合气体中NO与NO2的体积之比为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com