
分析 (1)根据C元素、H元素守恒确定该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2,2-二甲基丁烷,则该烃的结构简式为(CH3)3C-CH=CH2;
(2)根据2,5-二甲基已烷的结构可知,炔烃中的参键只能在3号碳和4号碳之间,据此确定炔的结构简式;
(3)饱和一元醇的分子式为CnH2n+2O,碱石灰增重的为二氧化碳和水的质量,结合该醇的物质的量计算出生成二氧化碳、水的物质的量及质量,然后列式计算出n,再根据“该醇不能进行催化氧化反应”确定其结构简式;
(4)苯酚与浓溴水反应生成三溴苯酚白色沉淀.
解答 解:(1)n(烃):n(C):n(H)=n(烃):n(CO2):2n(H2O)=0.1mol:0.6mol:0.6mol×2=1:6:12,即1个分子中含有6个C原子、12个H原子,故该烃的分子式为C6H12,在催化剂作用下与H2发生加成反应,生成2.2-二甲基丁烷,则该烃的结构简式为:(CH3)3C-CH=CH2,
故答案为:(CH3)3C-CH=CH2;
(2)根据2,5-二甲基已烷的结构可知,炔烃和H2充分加成生成2,5-二甲基已烷,炔烃中的参键只能在3号碳和4号碳之间,所以炔的结构简式为:(CH3)2CH-C≡C-CH(CH3)2,
故答案为:(CH3)2CH-C≡C-CH(CH3)2;
(3)设该饱和一元醇的分子式为CnH2n+2O,0.1mol该有机物完全燃烧生成0.1nmol二氧化碳、0.1(n+1)mol水,
碱石灰增重的质量为二氧化碳和水的质量,则:44g/mol×0.1nmol+18g/mol×0.1(n+1)mol=26.6g,解得:n=4,所以该饱和一元醇的分子式为:C4H10O,
该醇不能进行催化氧化反应,说明连接羟基的碳原子上不含H,故该饱和 一元醇的结构简式为:(CH3)3C-OH,
故答案为:(CH3)3C-OH;
(4)浓溴水与苯酚发生取代反应生成三溴苯酚沉淀,会观察到有白色沉淀产生,故答案为:产生白色沉淀.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握同分异构体的概念及书写原则,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 该合成中所有的电能和热能全部转化为化学能 | |
| B. | 该合成氨过程不属于氮的固定 | |
| C. | 空气、水、太阳能均为可再生资源 | |
| D. | 断裂N2中的N≡N键会释放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
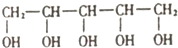 木糖醇原产于芬兰,是一种天热、健康的甜味剂,入口后往往伴有微微的清凉感,防龋齿,适合糖尿病患者的需要.它的结构简式如图.下列有关木糖醇的叙述错误的是( )
木糖醇原产于芬兰,是一种天热、健康的甜味剂,入口后往往伴有微微的清凉感,防龋齿,适合糖尿病患者的需要.它的结构简式如图.下列有关木糖醇的叙述错误的是( )| A. | 木糖醇易溶于水,溶解过程的△H>0 | |
| B. | 一定条件下,木糖醇能与HCl反应,也能与醋酸反应,属于同一反应类型 | |
| C. | 木糖醇是一种单糖,不能发生水解反应 | |
| D. | 1mol木糖醇与足量的钠反应最多可产生2.5molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
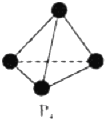 VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态.含VA族元素的化合物在研究和生回答下列问题:
VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态.含VA族元素的化合物在研究和生回答下列问题: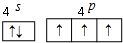 .N、P、As原子的第一电离能由大到小的顺序为N>P>As.
.N、P、As原子的第一电离能由大到小的顺序为N>P>As.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素最高价氧化物对应水化物的酸性一定强于Y | |
| C. | X与Y元素形成的两种常见化合物分别溶于水后溶液PH<7 | |
| D. | Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.80g Na2O2与5.85g NaCl所含阴离子数均为0.1NA | |
| B. | 一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA | |
| C. | 常温常压下,22.4LNH3所含分子数小于NA | |
| D. | 标准状况下,28g聚乙烯完全燃烧,产生的CO2数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com