
����Ŀ��������������˫��ˮ��ҽ������������ɱ��������������ϴ�˿ڣ�����˫��ˮ���ش��������⣺
A��Na2O2+2HCl=2NaCl+H2O2
B��Ag2O+H2O2=2Ag+O2��+H2O
C��2H2O2=2H2O+O2��
D��3H2O2+Cr2��SO4��3+10KOH=2K2CrO4+3K2SO4+8H2O
��1��������Ӧ�У�������������ԭ��Ӧ����__________������ţ���ͬ����H 2 O 2 �����ֻ�ԭ�Եķ�Ӧ��__________��
��2��������Ӧ˵��H2O2 ��Ag2O��K2CrO 4 ��������ǿ������˳����_________________
��3��ijǿ�ᷴӦ��ϵ�з�����һ��������ԭ�����ӷ�Ӧ����Ӧ��������ﹲ��������O2��MnO4�� ��H2O��Mn2+ ��H2O2 ��H+ ����֪�÷�Ӧ��H2O2 ֻ���������¹��̣�H2O2 ��O2��
�ٷ�Ӧ��ϵѡ������ǣ�____________ A������ B������ C����
�ڸ÷�Ӧ�����ӷ���ʽΪ________________________________________��
�����������Ӧ����2.24L����״�����������ɣ�ת�Ƶĵ���Ϊ _______mol��
��4��H2O2 ��ʱ����Ϊ��ҵ��Һ���������С���ɫ�������������ƣ��������ɿ�ҵ��Һ�е��軯���KCN���������·�Ӧʵ�飺KCN+H2O2 +H2O=A+NH3������ָ��������A�Ļ�ѧʽΪ_____________.
���𰸡� A B Ag2O>H2O2>K2CrO4 B 2MnO4��+ 5H2O2+16 H+= 2Mn2++ 8H2O + 5O2�� 0.2 KHCO3
��������(1)H2O2�����������ԣ���OԪ�صĻ��ϼ۽��ͣ�˫��ˮ�����ֻ�ԭ�ԣ�˵��˫��ˮ�ڷ�Ӧ�н������������ϼ�ֻ���ߣ�H2O2�����������������ֻ�ԭ�ԣ���OԪ�صĻ��ϼۼ������ֽ��ͣ�H2O2�Ȳ����������ֲ�����ԭ����˵���ڷ�Ӧ��˫��ˮ��Ԫ�صĻ��ϼ۲������仯��������Ӧ�У�Na2O2+2HCl=2NaCl+H2O2��û��Ԫ�صĻ��ϼ۷����仯�����ڷ�������ԭ��Ӧ��Ag2O+H2O2=2Ag+O2��+H2O ��H2O2�е�OԪ�ػ��ϼ�ֻ���ߣ�ֻ����H2O2�Ļ�ԭ�ԣ��ʴ�Ϊ��A��B��
(2)����B��Ag2O+H2O2=2Ag+O2��+H2O�������ԣ�Ag2O��H2O2������D��3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O�������ԣ�H2O2��K2CrO4����������ԣ�Ag2O>H2O2>K2CrO4 ���ʴ�Ϊ��Ag2O>H2O2>K2CrO4 ��
(3)�����ڸ���������Ӿ���ǿ�����ԣ��ܹ��������ᣬ���������ᣬ�����������ӱ�ʾ�����ֻ��ѡ�����ᣬ�ʴ�Ϊ��B��
��H2O2ֻ���������¹��̣�H2O2��O2����OԪ�صĻ��ϼ����ߣ�������������Ӧ����ԭ����ΪMnO4-��Mn2+�����������ӷ�ӦΪ2MnO4-+5H2O2+6H+�T2Mn2++5O2��+8H2O���ʴ�Ϊ��2MnO4-+5H2O2+6H+�T2Mn2++5O2��+8H2O��
��2.24L(��״��)�������ɣ���OԪ�صĻ��ϼ۱仯��֪��ת�Ƶ���Ϊ![]() ��2��(1-0)=0.2mol���ʴ�Ϊ��0.2��
��2��(1-0)=0.2mol���ʴ�Ϊ��0.2��
(4)KCN+H2O2+H2O�TA+NH3������ԭ���غ��֪AΪKHCO3���ʴ�Ϊ��KHCO3��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20mL0.1mol��L-1HA��Һ����μ���0.1 mol��L-1NaOH��Һ����pH�仯������ͼ��ʾ(�����¶ȱ仯)������˵���������

A. HA�ĵ��뷽��ʽΪHA![]() H++A-
H++A-
B. HA��ȫ��Ӧʱ����Һ����Ӧ�ĵ�λ��c��d֮��
C. �ζ���c��ʱ��c(Na+)>c(A-)>c(H+)=c(OH-)
D. �ζ���d��ʱ��n(Na+)+n(H+)-n(OH-)+n(HA)=0.002mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȷ�Ӧ��˵������ȷ����������
A. �����û���Ӧ B. ��������Ϊ������
C. ��Ӧ�зų��������� D. �����ں��Ӹֹ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CoC2O4���Ʊ������ܵ�ԭ�ϡ����ú��ܷ��ϣ���Ҫ�ɷ�ΪCo2O3��������Fe2O3��Al2O3��CaO��MgO��̼���л���ȣ���ȡCoC2O4�Ĺ����������£�
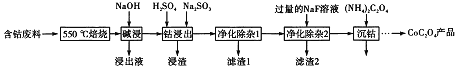
��1����500����������Ŀ����_______��
��2��������Һ������Ҫ�ɷ���_______��
��3�����ܽ�����������Co3+ת��ΪCo2+����Ӧ�����ӷ���ʽΪ_________��
��4������������1�������У�����40��50�� ����H2O2��Һ����Ŀ����_____________��
�������ӷ���ʽ��ʾ������������80��85��������Na2CO3��Һ����pH��5��������I������Ҫ�ɷ���___________��
��5������������2���ɽ��ơ�þ����ת��Ϊ�������˳�ȥ����������Һ��c(Ca2+)=1.0��10-5mol/L����c(Mg2+)Ϊ________����֪Ksp(MgF2)=7.35��10-11���� Ksp(CaF2)=1.05��10-10��
��6��Ϊ�ⶨ�Ƶõ�CoC2O4��Ʒ�Ĵ��ȣ��ֳ�ȡ1.00g��Ʒ���������ʵ��Լ�ת��Ϊ�����[(NH4��2C2O4����Һ�����ù���ϡ�����ữ����0.1000mol/L���������Һ�ζ�����_________ʱ�����ﵽ�ζ��յ㣬����ȥ���������Һ26.00mL���ò�Ʒ�Ĵ���Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CH4�ں�ѹ�ܱ������з�����Ӧ��CH4(g)![]() C(s) + 2H2(g)��ƽ��ʱ����ϵ�и���������������¶ȵĹ�ϵ��ͼ��ʾ��
C(s) + 2H2(g)��ƽ��ʱ����ϵ�и���������������¶ȵĹ�ϵ��ͼ��ʾ��
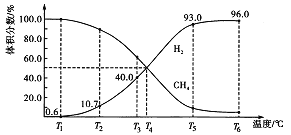
��1����֪���顢̼��������ȼ���ȷֱ�Ϊ890.31kJ/mol��395.00kJ/mol��285.80kJ/mol����÷�Ӧ�ķ�Ӧ����H=__________��
��2��������˵����Ӧһ���ﵽƽ��״̬����_______��
a.H2��CH4������������ b����������ƽ����Է�����������
c�����������ܶȲ��� d��������ѹǿ���ٱ仯
e��̼���������ٸı�
��3��T2��ʱ������ƽ����ϵ�г���������壬��ʱ��Ӧ����________�����������������С������������������v��_______v��(����>������<������=��)��
��4��T4��ʱ������ƽ����ϵ�г���������H2��CH4����ƽ��_____�ƶ�����������_______��
��5��T3��ʱ����Ӧ��ƽ���CH4��ת����Ϊ____________��
��6��CH4�ܴ�����ת��ΪCO��H2����ͼ��һ������̼����ȼ�ϵ��ʾ��ͼ���缫A��CO����缫��Ӧ����ʽΪ____________________��
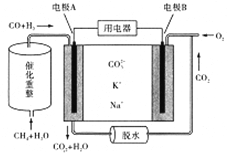
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֳּ����ǻ������ݲɼ������������Ͷ�ý���������ɵ�һ��������������ϵͳ������ʵʱ��������ֱ�۵��ص㣬ͼ2�������ֳּ����õ����������ʵ����ı仯ͼ����������20mL 0.2mol/L H2A��Һ�еμ�0.2mol/L NaOH��Һ�����Т����H2A�������HA- �������A2-,����˵����ȷ���ǣ� ��
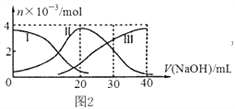
A. H2A��ˮ�еĵ��뷽��ʽ�ǣ�H2A�T2H++A2-
B. ��V��NaOH��=40mLʱ������Һ��ˮ�ĵ����ܵ�����
C. ��V��NaOH��=20mLʱ�����У�c��Na+����c��HA-����c��H+����c��A2-����c��OH-��
D. ��V��NaOH��=30mLʱ�����У�c��H+�� +c��Na+���T c��A2-��+ c��OH-��+ c��HA-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����м���CO32-���õ��Լ��ǣ� ��
������ ��NaOH��Һ �۳����ʯ��ˮ
A. �٢�B. �٢�C. �ڢ�D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ص�ԭ����������ij�ֳ������ϼ۵Ĺ�ϵͼ������ԭ��������������Ӧ��Ԫ�أ�������˵����ȷ����
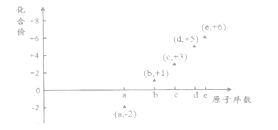
A. ��ҵ�ϳ��õ�ⷨ�Ʊ�����b��c B. 31d��33d����ͬ�ֺ���
C. ��̬�⻯����ȶ��ԣ�d>a>e D. a��b�γɵĻ����ﲻ���ܺ����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л������ڷӵ��ǣ� ��
A. C6H5��CH2OHB. HO��C6H4��CH3
C. C2H5��OHD. C6H5��CH2CH2OH
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com