
| A. | L层上的电子数为奇数的原子一定是主族元素的原子 | |
| B. | 核电站泄漏的放射性物质131I和127I互为同位素,化学性质相似 | |
| C. | 化学键的形成一定伴随着电子的转移和能量变化 | |
| D. | 元素周期表中,位于金属和非金属分界线附近的元素属于过渡元素 |
分析 A、L层上的电子数为奇数的原子,只有2个电子层;
B、质子数相同中子数不同的同一元素的不同原子互称同位素,同位素化学性质相似;
C、同素异形体之间的转化不存在电子转移;
D、过渡元素包含副族元素与第Ⅷ族元素.
解答 解:A、L层上的电子数为奇数的原子,只有2个电子层,为第二周期ⅠA、ⅢA、ⅤA、ⅤⅡA族元素,则一定为主族元素的原子,故A正确;
B、131I与127I相同质子数相同,中子数不同,互称同位素,化学性质相似,故B正确;
C、同素异形体之间的转化不存在电子转移,故C错误;
D、过渡元素包含副族元素与第Ⅷ族元素,位于金属和非金属分界线附近的元素为半导体元素,故D错误;
故选AB.
点评 本题考查原子结构、元素周期表与周期律等,难度不大,C选项为易错点,注意特殊反应.


科目:高中化学 来源: 题型:选择题
| A. | 向NaHSO3溶液中加入NaHSO4溶液:HSO${\;}_{3}^{-}$+H+═H2O+SO2↑ | |
| B. | 铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| C. | Ba(OH)2与H2SO4两稀溶液混合:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个Na+的Na2OH溶解于1L水中,Na+浓度为1mol•L-1 | |
| B. | 常温常压下,11.2LH2 中含有分分子数大于0.5NA | |
| C. | 常温常压下,30.8gCCl4中含有的原子数目为NA | |
| D. | 2L0.5mol•L-1H2O2溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
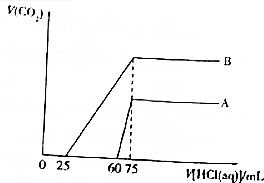 取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,再分别向稀释后的溶液中逐滴加入0.1mol•L-1的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如图所示.
取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,再分别向稀释后的溶液中逐滴加入0.1mol•L-1的盐酸,标准状况下产生CO2气体体积与所加盐酸体积之间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下在水中溶解性比KHCO3>K2CO3 | |
| B. | 热稳定性K2CO3<KHCO3 | |
| C. | 和酸反应放出CO2的快慢KHCO3>K2CO3 | |
| D. | 等量的盐酸分别与足量KHCO3和K2CO3反应,产生CO2一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的水溶液可以导电,CO2是电解质 | |
| B. | 硫酸钡难溶于水,但却是电解质 | |
| C. | 氯化钠溶液在电流的作用下电离成钠离子和氯离子 | |
| D. | 溶于水后能电离出氢离子的化合物都是酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com