
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法正确的是
A.气体A是NO2
B.X中肯定存在Fe2+、A13+、NH4+、SO42―
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是 A13+和C1―
D
【解析】
试题分析:pH=1的溶液为酸性溶液,在酸性溶液中,CO32―、SO32―不能存在;X溶液与过量硝酸钡溶液反应产生气体、沉淀,且该气体可连续与氧气反应,说明是硝酸与溶液中的还原性离子发生氧化还原反应,则溶液中一定存在亚铁离子,则A是NO,D是二氧化氮,E是硝酸;沉淀C是硫酸钡,说明溶液中一定存在硫酸根离子;溶液B中至少含有硝酸钡、硝酸铁;B中再加入氢氧化钠溶液加热产生气体,说明原溶液中一定存在铵根离子,F是氨气;因为氢氧化钠是过量的,且溶液B中存在铁离子,所以沉淀G中一定有氢氧化铁;溶液H中至少含有氢氧化钠、硝酸钠、氢氧化钡,通入二氧化碳,未指明二氧化碳的量的多少,所以产生的沉淀I的成分不能确定,若二氧化碳少量则I中含有碳酸钡,可能有氢氧化铝,所以铝离子不能确定,同时氯离子也不能确定。溶液E是硝酸与氨气可发生反应,所以正确答案选D。
考点:考查离子的检验,离子反应的判断


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:选择题
根据原子结构及元素周期律的知识,下列推断正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.还原性强弱: F- < Cl- < I-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:填空题
(本题共12分)磷单质及其化合物在工业生产中有着广泛的应用。白磷可用于制备高纯度的磷酸(磷酸结构式为 ),次磷酸钠(NaH2PO2)可用于化学镀镍等等。
),次磷酸钠(NaH2PO2)可用于化学镀镍等等。
完成下列填空:
23.NaH2PO2中涉及到四种元素,它们的原子半径由小到大的顺序为____________。
24.写出与磷同周期的主族元素中,离子半径最小的元素,其最高价氧化物对应水化物的电离方程式______。
25.磷酸二氢钠主要用于制革、处理锅炉水及在食品工业、发酵工业中作缓冲剂。其水溶液呈酸性的原因是_______________________________________________________。(请用文字描述)
26.已知磷酸分子中的三个氢原子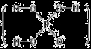 都可以跟重水分子(D2O)中的D原子发生氢交换。 又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是
都可以跟重水分子(D2O)中的D原子发生氢交换。 又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是

27.次磷酸钠(NaH2PO2)可用于化学镀镍。化学镀镍的溶液中含有Ni2+和H2PO2-,在一定条件下能发生如下反应:__Ni2++__H2PO2-+ →__Ni + ___H2PO3-+_____。请完成并配平上述反应离子方程式。该反应的还原产物是__________,反应中转移1摩尔电子时,理论上产生金属镍______克。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:选择题
晶体的叙述中,正确的是
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间的作用力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.离子晶体不一定能溶于水,但一定不含非极性共价键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省五校高三第一次模拟联考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的能级,且每种能级中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N的质荷比最大值为78;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同。
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)化合物M的空间构型为 ,其中心原子采取 杂化;化合物N在固态时的晶体类型为 。
(2)R、X、Y三种元素的第一电离能由小到大的顺序为 。
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为 (写分子式)。
(4)Z原子基态时的外围电子排布式为 ;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为 。

(5)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质。该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省五校高三第一次模拟联考理综化学试卷(解析版) 题型:选择题
短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:
① R、Y原子的最外层电子数与电子层数相同;
② Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;
③ W与R同主族。下列说法正确的是
A.元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型
B.元素T、Q、W、Y的原子半径大小为:T<Q<Y<W
C.Q与Y组成的常见物质是一种两性物质,结构中含有共价键
D.由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省等四校高三第二次联考化学试卷(解析版) 题型:填空题
(10分)有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y单质晶体熔点高硬度大。试回答下列问题:
(1)五种元素中原子半径最大的元素是__________(写元素符号)
(2)X与M两元素以原子个数1:1形成的化合物的电子式为____________________
(3)写出由YM2制取Y单质的化学方程式____________________
(4)化合物Z 2 W 2遇水剧烈反应,产生黄色沉淀和刺激性气味的气体,其反应的化学方程式为____________
(5)W、M两元素形成的单质和化合物常用来杀菌消毒,试举例__________(写化学式,任写两种)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东师大附中高三第四次模拟考试理综化学试卷(解析版) 题型:填空题
(12分)下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。反应①常被应用于野外焊接钢轨,②是工业上重要的反应之一。
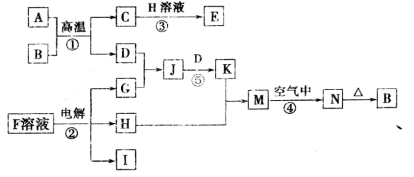
请回答下列问题:
(1)H中含有的化学键类型是________________________。
(2)上述框图所示的反应中,既属于化合反应,又属于氧化还原反应的反应共有______个;反应③的离子方程式____________________________。
(3)25℃时,以Pt为电极电解含有少量酚酞的F的饱和溶液,若在溶液变红的一极收集到0.2 g气体,则此时溶液的pH是_______(假设溶液的体积为2 L且不考虑电解后溶液体积的变化)。
(4)J溶液显_______(填“酸”、“碱”或“中”)性,原因是_________________________。(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三1月检测化学试卷(解析版) 题型:选择题
等体积等浓度的MOH强碱溶液和HA弱酸溶液混和,溶液中离子浓度关系不正确的是
A.c(M+)=c(HA)+c(A-) B.c(M+)>c(H+)>c(A-)>c(OH-)
C.c(OH-)=c(H+)+ c(HA) D.c(M+)+c(H+) =c(OH-)+c(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com