
VmL Al2(SO4)3溶液中含A13+ag,取V/5 mL该溶液稀释到5VmL,则稀释后溶液中SO42—的物质的量浓度是( )。
A.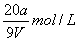 B.
B.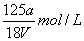 C.
C. D.
D.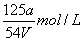
科目:高中化学 来源: 题型:
常温下,四种溶液的pH如下表:

下列说法正确的是
A. 在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变
B. 将V1 mL④溶液与V2mL②溶液混合后,测得混合溶液pH=4,则V1:V2=9:11
C. 分别加水稀释10倍,四种溶液的pH大小顺序为①〉②〉③〉④
D. 将①、④两种溶液等体积混合,所得溶液中•
查看答案和解析>>
科目:高中化学 来源: 题型:
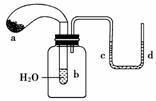
如右图所示,试管中盛有水,气球a中盛有干燥的Na2O2粉末,U形管中注有浅红色的水。将气球用橡皮绳紧系在试管口。实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是
A.U形管内的红水退色 B.试管内溶液变红
C.气球a被吹大 D.U形管中的水位:c端高于d
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.在标准状况下,体积为22.4L的物质都是1mol
B.在非标状况下,1mol任何气体的体积不可能是22.4L
C.在标准状况下,1mol H2O和1mol H2的体积都为22.4L
D.同温同压下两种气体,只要它们的分子数相同 ,所占体积也一定相同
,所占体积也一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对0.2mo1/LNa2SO4溶液叙述不正确的是(NA表示阿伏加德罗常数的值)( )
A. 1L溶液中含0.4NA个Na+ B.1L溶液中含Na+和SO42-总数为0.8NA
C.2L溶液中含有0.4NA个SO42- D. 2L溶液中Na+的物质的量浓度为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制500 mL、0.2 mol·L-1的稀硫酸。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平⑦容量瓶⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2)经计算,需浓H2SO4的体积为 。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是 (填代号)
(3)在配制过程中,其他操作都准确,下列操作中:
错误的是 ,能引起所配溶液浓度偏高的有 (填代号)。
①转移溶液后,未洗涤烧杯和玻璃棒
②转移前,容量瓶中含有少量蒸馏水
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线
(4)将250mL0.2 mol·L-1稀硫酸与足量的Na2CO3充分反应,在标准状况下可得 升CO2。
查看答案和解析>>
科目:高中化学 来源: 题型:
某苯的同系物分子式为C11H16,经分析分子中除含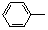 外,不再含其他环状结构,还含有3个—CH3、1个—CH2—、1个
外,不再含其他环状结构,还含有3个—CH3、1个—CH2—、1个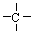 ,它可能的结构有( )
,它可能的结构有( )
A. 1种 B.2种 C.3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验操作或事故处理方法正确的是 ( )
A.酒精灯着火时可用水扑灭
B.为防止试管破裂,加热固体时试管口一般要略高于试管底
C.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,边搅拌条件下边加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO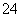 -2e-===PbSO4
-2e-===PbSO4
正极PbO2+4H++SO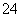 +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式
_____________________。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为________极。
(3)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1. 15 g/cm3)时,
①若收集到11.2L(标准状况下)氯气,则至少转移电子________mol。
②若铅蓄电池消耗H2SO42 mol,则可收集到H2的体积(标准状况下)为________L。
③若消耗硫酸a mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)________(用含a的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com