
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源。
(1)设汽油成分为C8H18,若在气缸中汽油高温裂解产生丁烷和丁烯,写出该反应的化学方程
▲ 。
(2)气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0
2NO(g) △H >0
①汽车启动后,气缸内温度越高,单位时间内NO排放量越大,原因是 ▲ 。
②1mol空气中含有0.8molN2和0.2molO2,1300℃时在含1mol空气的密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K≈ ▲ 。
(3)尾气中的CO主要来自于汽油不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g) △H=+221kJ·mol-1,简述该设想能否实现的依据: ▲ 。
②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用下图简单表示,则阳极发生的电极反应为 ▲ 。

(4)在汽车尾气系统中安装催化转换器,可有效减少尾气中的CO、NOx 和碳氢化合物等废气。
已知:N2(g)+O2(g)=2NO(g) △H1=+180kJ/mol
CO(g) +1/2O2(g)= CO2(g) △H2=-283kJ/mol
2NO(g)+ 2CO(g) = 2CO2(g) + N2(g) △H3
则△H3 = ▲ kJ·mol-1。
(5)光化学烟雾(含臭氧、醛类、过氧乙酰硝酸酯等)是汽车尾气在紫外线作用下发生光化学反应生成的二次污染物。写出2-丁烯与臭氧按物质的量之比为1:2反应生成乙醛及氧气的化学方程式 ▲ 。
科目:高中化学 来源: 题型:
铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况
下体积相等时,反应中消耗的盐酸和氢氧化钠物质的量之比为
A.3:1 B.2:1 C.1:1 D,1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
可用来鉴别己烯、苯酚、甲苯、乙酸乙酯溶液的一组试剂是( )
A.氯化铁溶液、溴水 B.碳酸钠溶液、溴水
C.KMnO4酸性溶液、溴水 D.KMnO4酸性溶液、氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据相关实验得出的结论正确的是
| 选项 | 实验步骤 | 现象 | 结论 |
| A | 浓硫酸与乙醇加热,产生的气体X直接通入溴水 | 溴水褪色 | X一定是纯净的乙烯 |
| B | 溴乙烷、乙醇及固体NaOH混合加热,产生的气态物质Y,直接通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | Y一定是纯净的乙烯 |
| C | 在含有酚酞的Na2CO3溶液中加入适量BaCl2溶液振荡 | 红色褪去 | 说明Na2CO3溶液中存在水解平衡 |
| D | Z、W两试管中分别盛有pH和体积相同的盐酸和醋酸溶液,同时分别投入质量大小、形状相同的少量锌粒 | Z中产生气体速率快 | Z中盛放的是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
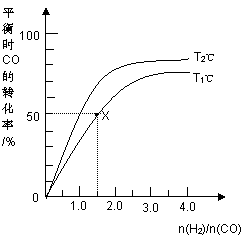
在2L的密闭容器中,起始时均投入2molCO,在不同条件下发生反应:CO(g) +2H2(g)  CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
A.T1<T2
B.T1℃时该反应的平衡常数为4.0 L2·mol-2
C.同一温度下,n(H2)/n(CO)越大,平衡常数也越大
D.相同条件下n(H2)/n(CO)越大,CO和H2的转化率也越大
查看答案和解析>>
科目:高中化学 来源: 题型:
(已知某烃A含碳元素的质量分数为85.7%。结合以下信息回答问题:
(1).若烃A密度是相同状况下氢气密度的42倍。则烃A的相对分子质量_____________,分子式为_____________。
(2). 若烃A可作果实催熟剂。
则由A制取高分子化合物的化学方程式为
A和水在一定条件下反应生成B,B为生活中常见的有机物,B可与另一种生活中常见有机物在一定条件下反应生成有香味的物质C,写出生成C的化学方程式
。
比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。乙烯和氯化氢在一定条件下制得氯乙烷的化学反应方程式是(有机物用结构简式表示) ,该反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,某一密闭恒容的容器内有可逆反应:A(g)+3B(g)  2C(g)。
2C(g)。
该反应进行到一定限度后达到了化学平衡,该化学平衡的标志是 ( )
A.C物质的生成速率和分解速率相等
B.容器内气体的密度不再随时间而改变
C.单位时间内生成a mol物质A,同时生成3a mol物质B
D.A、B、C三种物质的分子数之比为1:3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com