

| ||
| ||
| 0.336L |
| 22.4L/mol |
| 0.03mol |
| 5-2 |
| 0.11mol |
| 1L/mol |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | +2 | -2 |
| A��R���������Ӧ��ˮ������ܾ������� |
| B��L��Q�γɵļ����Ӻ����������� |
| C��T��Q���⻯�ﳣ̬�¾�Ϊ��ɫ���� |
| D��L��M�ĵ�����ϡ���ᷴӦ���ʣ�M��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |
| ʵ����� | �¶ȡ� | ��ʼCCl4Ũ�ȣ�mol?L-1�� | ��ʼH2Ũ�ȣ�mol?L-1�� | CCl4��ת���� |
| 1 | 110 | 0.8 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | K+��Ba2+Fe2+Al3+ Fe3+ Mg2+ | ||||
| ������ | OH-HCO
|
- 3 |
2- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
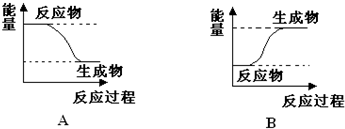
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO��CO2���Ԫ����ͬ�����ܽ�Fe2O3��ԭ��Fe |
| B��SiO2��CO2��Ϊ���������������NaOH��Һ��Ӧ������ |
| C��Na2O��Na2O2Ϊ��ͬԪ����ɵĽ���������� CO2��Ӧ������ͬ |
| D��Ũ���ᡢŨ���ᡢϡ���������ǿ�����ԣ������¾�������������ʢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A������ag��C2H4��C3H6�Ļ�����й��õ��Ӷ���ĿΪ
| ||
| B�������£�pH=13��NaOH��Һ�к���OHһ����ĿΪ0.1NA | ||
| C�����³�ѹ�£�14g��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪ2NA | ||
| D��1L 1mol?L-1��NaClO ��Һ�к���ClO-����ĿΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com