
| A. | 平衡向正反应方向移动 | B. | A的转化率增大 | ||
| C. | m+n<p | D. | C的体积分数增加 |
分析 mA(g)+nB(g)?pC(g),达到平衡后,温度不变,将气体体积压缩到一半,若平衡不移动,C的浓度为原来的2倍,当达到平衡时C的浓度为原来的2.1倍,则体积减小时平衡正向移动,以此来解答.
解答 解:A.由上述分析可知,平衡向正反应方向移动,故A正确;
B.平衡向正反应方向移动,则A的转化率增大,故B正确;
C.体积缩小,相当于加压,平衡正向移动,则m+n>p,故C错误;
D.平衡正向移动,则C的体积分数增加,故D正确.
故选C.
点评 本题考查化学平衡移动的影响,为高频考点,侧重于学生的分析能力的考查,题目难度不大,本题注意用假定法判断,如果平衡不移动,则达到平衡时C的浓度为原来的2倍,根据实际C的浓度,判断平衡移动.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4的摩尔质量是98g/mol | |
| B. | 2 mol H2O和2 mol NH3含电子数相同 | |
| C. | 等质量的O2和O3中所含氧原子个数不同 | |
| D. | 等物质的量的CO和CO2中所含碳原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过电泳实验证明胶体带电 | |
| B. | 通常利用丁达尔效应区别溶液与胶体 | |
| C. | 过滤实验说明胶体粒子不能透过滤纸 | |
| D. | 向煮沸的NaOH溶液中滴加FeCl3溶液可制备Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 编号 | C(H2)mol/L | C(CO)mol/L |
| 甲 | 2 | 1 |
| 乙 | 1 | 2 |
| 丙 | 1 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
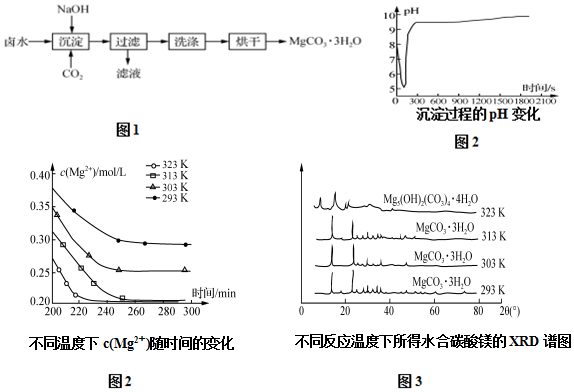
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡膳食就是各种食物都要吃 | |
| B. | 摄入食物中的营养素种类齐全,数量充足,比例适当且与人体的需要的保持平衡才是合理的膳食结构 | |
| C. | 淀粉、油脂、蛋白质为人体提供热能,所以只要这三种摄入量足够就可以了 | |
| D. | 麦芽糖不可以水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com