
现有由等质量的NaHCO3和KHCO3组成的混合物a g,与100 mL盐酸反应。(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示。)
(1)该混合物中NaHCO3与KHCO3的物质的量之比为________。
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量为________mol。
(3)如果盐酸过量,生成CO2的体积为________L;
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道__________ _______________________________________________。
_______________________________________________。
(5)若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是 ________________。
________________。
解析 (1)质量相等时,物质的量与摩尔质量成反比,所以二者的物质的量之比是100∶84(或25∶21)。
(2)混合物中NaHCO3和KHCO3的物质的量分别为 mol与
mol与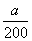 mol,则根据离子方程式HCO3-+H+===H2O+CO2↑可知,HCl的物质的量是
mol,则根据离子方程式HCO3-+H+===H2O+CO2↑可知,HCl的物质的量是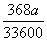 mol
mol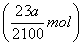 。
。
(3)根据碳原子守恒或反应方程式可知,生成CO2的体积是 L。
L。
(4)由于盐酸不足,则生成的CO2需要以HCl的物质的量进行计算。因此还需要知道盐酸的物质的量浓度。
(5)可以采用极值法进行计算,如果全部是碳酸氢钠,则生成CO2的体积是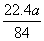 L;如果全部是碳酸氢钾,则生成的CO2的体积是
L;如果全部是碳酸氢钾,则生成的CO2的体积是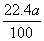 L,所以
L,所以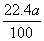 L<V(CO2)<
L<V(CO2)<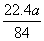 L。
L。
答案 (1)100∶84(或25∶21) (2)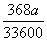
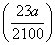
(3) (4)
(4) 盐酸的物质的量浓度(其他合理答案也可) (5)
盐酸的物质的量浓度(其他合理答案也可) (5)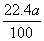 L<V(CO2)<
L<V(CO2)<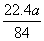 L
L


科目:高中化学 来源: 题型:
下列叙述中,错误的是
A.H2S、H2O、HF的稳定性依次增强
B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Ca、Mg、Na的还原性依次减弱
D.H2SiO3、H2CO3、H2SO4的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
有关物质的结构和组成如图所示,下列说法中不正确的是 ( )
|


A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
B.该气态团簇分子(图乙)的分子式为EF或FE
C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D.在碘晶体(图丁)中,碘分子的排列有两种不同的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱 原理制取Na2CO3的流程图。
原理制取Na2CO3的流程图。

已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐 酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是_________________________ _________________________________________________________________。
(2)灼烧固体A制Na2CO3在________(填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是_____________________________________ _________________________________________________________________。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为____________________。
(3)下图装置中常用于实验室制备CO2的是________(填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是________(填试剂名称),烧瓶内可加入的固体试剂是________(填试剂名称)。
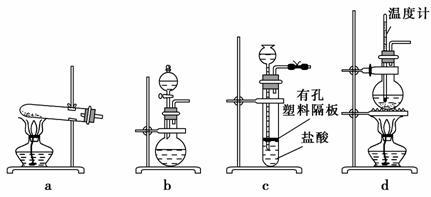
(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4 溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
②_______________________________________________________________。
③_______________________________________________________________。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )。
)。
A.等质量的N2和CO所含分子数均为NA
B.在标准状况下,22.4 L CH4与18 g H2O所含的电子数均为10NA
C.一定温度下,1 L 1 mol·L-1的CH3C OONa溶液含NA个CH3COO-
OONa溶液含NA个CH3COO-
D.1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是( )
①用铜作电极电解饱和NaCl溶液,当线路中通过NA个电子时,阳极产生11.2 L气体(标准状况下) ②常温常压下,16 g O2和16 g O3含氧原子数均为NA ③标准状况下,22.4 L CH3CH2OH中含有的碳原子数为2NA ④6.5 g锌全部溶于一定量的浓硫酸,生成SO2与H2的混合气体,气体分子总数为0.1NA ⑤10.6 g Na2CO3粉末中含有CO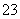 数为0.1NA
数为0.1NA
A.②④⑤ B.①③⑤
C.①②④⑤ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
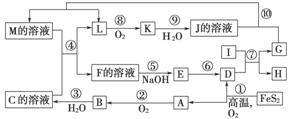
提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是
______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素比硫元素非金属性强的是 ( )
①HCl比H2S稳定;②HClO4酸性比H2SO4强;③Cl2能与H2S反应生成S;④Cl原子最外层有7个电子,S原子最外层有6个电子;⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS;⑥盐酸是强酸,而氢硫酸是弱酸
A.①②③④⑤⑥ B.①②③④⑥ C.①②③⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐主要成分是NaCl,还含有SO42-等其他可溶性杂质离子。下列说法不正确的是
A.除去SO42- 最合适的试剂是BaCl2
B.工业上通过电解氯化钠溶液制备金属钠和氯气
C.室温下,AgCl在水中的溶解度大于在食盐水中的溶解度
D.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com