
| A. | (2)(4)(5) | B. | (2)(7) | C. | (1)(3)(4) | D. | (5)(6)(7) |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:(1)C的生成速率与C的分解速率相等,正逆反应速率相等达平衡状态,故正确;
(2)单位时间内amol A生成,同时生成3amol B,都体现的逆反应方向,故错误;
(3)A、B、C的浓度不再变化,说明达平衡状态,故正确;
(4)混合气体的总压强不再变化,说明各物质的量不变,反应达平衡状态,故正确;
(5)混合气体的物质的量不再变化,说明各物质的量不变,反应达平衡状态,故正确;
(6)单位时间消耗amol A,等效于消耗3amol B,同时生成3amolB,正逆反应速率相等,反应达平衡状态,故正确;
(7)平衡时A、B、C的分子数目比可能为1:3:2,也可能不是,故错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


科目:高中化学 来源: 题型:填空题
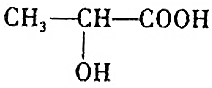 的反应(官能团羟基、羧基,具有醇和酸的性质)
的反应(官能团羟基、羧基,具有醇和酸的性质)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验:
某天然碱样品的组成可能为aNa2CO3•bNaHCO3•cH2O(a、b、c为正整数).为确定其组成,某小组进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与硫酸反应:Cu(OH)2+2H+=Cu2++2H2O | |
| B. | 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 氯化钡溶液与硫酸反应:Ba2++SO42-=BaSO4↓ | |
| D. | 氧化铜与硫酸反应:CuO+2H+=Cu2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和O3 | B. | ${\;}_{1}^{2}$H和${\;}_{1}^{2}$H | ||
| C. | 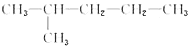 和CH3-CH2-CH2-CH2-CH2-CH3 和CH3-CH2-CH2-CH2-CH2-CH3 | D. | CH3-CH2-CH3和CH3-CH2-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2.8H2O与NH4Cl反应 | B. | 钠与冷水的反应 | ||
| C. | 灼热的炭与CO2反应 | D. | 甲烷与O2的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
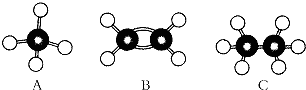
 、
、 .
.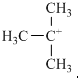 ,它是有机反应中重要的中间体,
,它是有机反应中重要的中间体,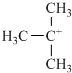 失去一个H+后将生成B的同系物F,F的结构简式为
失去一个H+后将生成B的同系物F,F的结构简式为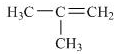 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com