
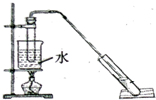
 �����dzµ��㡱������Ϊ���ڴ������������������ζ������������ij��ȤС������ˮ�Ҵ��ͱ������Ʊ�����������������ʵ��������£�
�����dzµ��㡱������Ϊ���ڴ������������������ζ������������ij��ȤС������ˮ�Ҵ��ͱ������Ʊ�����������������ʵ��������£�| ���� | �Ҵ� | ���� | �������� |
| ������ | 46 | 60 | 88 |
| �е㣨�棩 | 78.5 | 117.9 | 77.1 |
| �ܶȣ�g/cm3�� | 0.789 | 1.05 | 0.90 |
���� ��1���������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ����Ϸ�Ӧ�ص�ȷ����Ӧ���ͣ�Ũ�����Ǵ�������ˮ����
��2���ӷ�ʯ���Է�ֹ���У�ˮԡ���ȿ���ʹ���Ⱦ��ȣ������ܵ�����������������
��3������̼���Ƶ������������Ҵ��������ᷴӦ��ȥ���ᡢͬʱ���������������ܽ�ȣ����ڷֲ㣻
��4�����ݷ�Һ�����Լ���Һ©����ʹ���ص����ش�
��5������=$\frac{ʵ������}{��������}$��100%��
��6�����淴Ӧ���ܽ�����ȫ���ݴ˻ش�
��� �⣺��1���������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOC2H5+H2O������ȡ����Ӧ��Ũ�����ڴ˷�Ӧ�е������Ǵ�������ˮ����
�ʴ�Ϊ��CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOC2H5+H2O��ȡ����Ӧ����������ˮ����
��2���ӷ�ʯ���Է�ֹ���У�ˮԡ���ȿ���ʹ���Ⱦ��ȣ������ܵ������������������ʴ�Ϊ����ֹ���У����Ⱦ��ȣ�����������
��3��������������ʱ���ñ���̼������Һ��Ŀ�����кͻӷ����������ᣬʹ֮ת��Ϊ����������ˮ�У�������������������ζ���ܽ�ӷ��������Ҵ�����������������ˮ�е��ܽ�ȣ����ڷֲ�õ�����
��ѡBD��
��4����Һ��Ҫ�õ��Ĺؼ������Ƿ�Һ©�������������ܶ�С���ڷ�Һ©�����ϲ㣬Ӧ�ôӸ��������ϲ��������ʴ�Ϊ����Һ©�����ϲ�������
��5�������Ҵ���������0.789��3g=2.367g����������������1.05��2g=2.1g�����Ի����Ҵ�ʣ�࣬����ȫ����Ӧ��
CH3COOH+C2H5OH$?_{��}^{Ũ����}$CH3COOC2H5+H2O��
60 46 88
2.1g
���۲�����������������=$\frac{88��2.1}{60}$g=3.08g�����Բ���=$\frac{2.3��0.9}{3.08}$��100%��67.2%���ʴ�Ϊ��67.2%��
��6����ʵ���У�����3mol�Ҵ���1mol���ᣬ��Ũ���������¼��ȣ���ַ�Ӧ��������1mol������������Ϊ�������������ķ�Ӧ�ǿ��淴Ӧ��1mol�������ȫ��������
�ʴ�Ϊ�����ܣ��÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ������ȫת���������
���� ���⿼���������������Ʊ����������淴Ӧ�ص㣬��Ŀ�Ѷ��еȣ�ע���������������ķ�Ӧԭ�����Ʊ���������ȷ���淴Ӧ�ص㣬Ũ���ᡢ����̼������Һ����������������Ӧ�е�����Ϊ������ȵ㣬Ҫ��ѧ���������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol NH3�����еĵ�����Ϊ17NA | |
| B�� | ���³�ѹ�£�22.4 L����������ԭ����Ϊ2NA | |
| C�� | ���³�ѹ�£�48g O3��������ԭ����Ϊ3NA | |
| D�� | 1 mol/L NaCl��Һ��������Na+��ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
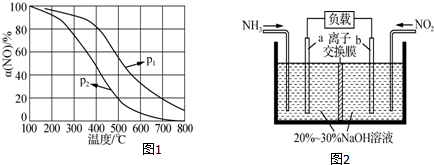
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
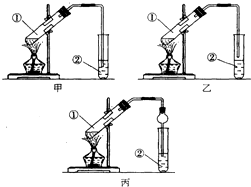 �����Ǽס��ҡ�����λͬѧ��ȡ���������Ĺ��̣�������벢Э������������ʵ������
�����Ǽס��ҡ�����λͬѧ��ȡ���������Ĺ��̣�������벢Э������������ʵ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiH4�ķе����CH4���Ʋ�HCl�ķе����HF | |
| B�� | Fe��CuSO4��Һ��Ӧ�û���Cu����NaҲ�ܴ�CuSO4��Һ���û���Cu | |
| C�� | �������NaCl��ȡNa���ʵ������MgCl2Ҳ����ȡMg | |
| D�� | CO2��Na2O2��Ӧ����Na2CO3��O2����SO2��Na2O2��Ӧ����Na2SO3��O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼúʱ��������ʯ��ʯ���ɼ��ٷ�����SO2���� | |
| B�� | �����������������10-4%�Ŀ������������彡�� | |
| C�� | CO��NO��NO2���Ǵ�����Ⱦ���壬�ڿ����ж����ȶ����� | |
| D�� | ���ϳ�ϴ�Ӽ����ڱ�ϸ���ֽ⣬�ʲ��ᵼ��ˮ����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com