
| A. | 少量AlCl3溶液滴入过量的NaOH溶液中:Al3++4OH-=AlO2-+2H2O | |
| B. | 将一小块金属钠投入到硫酸铜溶液中:2Na+Cu2+=Cu+2Na+ | |
| C. | FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+ | |
| D. | 氯气溶解于水:Cl2+H2O?2H++Cl-+ClO- |
分析 A.氯化铝少量反应生成偏铝酸钠和水;
B.不符合反应客观事实;
C.电荷不守恒;
D.次氯酸为弱酸应保留化学式.
解答 解:A.少量AlCl3溶液滴入过量的NaOH溶液中,离子方程式:Al3++4OH-=AlO2-+2H2O,故A正确;
B.钠先与水反应生成氢氧化钠与氢气,氢氧化钠再与硫酸铜反应生成氢氧化铜沉淀与硫酸钠,反应总的离子方程式为2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑,故B错误;
C.FeCl3溶液与Cu反应,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故C错误;
D.氯气溶解于水,离子方程式:Cl2+H2O?H++Cl-+HClO,故D错误;
故选:A.
点评 本题考查离子方程式的书写与正误判断,难度中等,是对学生综合能力与所学知识运用的考查,掌握元素化合物知识与离子方程式的书写与判断方法是解题关键,注意化学式拆分,注意离子反应遵循客观事实.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “海水淡化”可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 | |
| B. | 漂白粉解决了氯水漂白时不稳定、难以保存、使用不方便、效果不理想的问题 | |
| C. | 钢铁的腐蚀最普遍的是吸氧腐蚀,最终产物为铁锈 | |
| D. | 温度、压强一定时,放热且熵增的反应能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
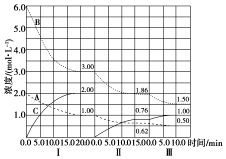 已知某放热热反应在1L的密闭容器中进行反应.保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如图所示:
已知某放热热反应在1L的密闭容器中进行反应.保持容器体积不变,改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各气体物质浓度随时间变化的曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>2c | B. | a=b<2c | C. | b=2c=a | D. | b=2c<a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | SO2具有漂白性 | SO2可用于食品增白 |
| B | SiO2熔点高 | SiO2可用于制作耐高温仪器 |
| C | Al(OH)3具有弱碱性 | Al(OH)3可用于制胃酸中和剂 |
| D | Fe3+具有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol氯气参加氧化还原反应时电子转移数一定是2NA | |
| B. | 常温常压下,56 g Fe与足量的盐酸完全反应转移的电子数为3NA | |
| C. | 同温同压下,等质量的H2和O2的体积之比是16:1 | |
| D. | 1mol的Na2O2固体中含有离子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
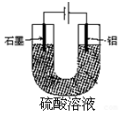 铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( )| A. | 阳极电极方程式为Al-3e+6OH-=Al2O3+3H2O | |
| B. | 随着电解的进行,溶液的pH逐渐增大 | |
| C. | 当阴极生成气体3.36L(标况)时,阳极增重2.4g | |
| D. | 电解过程中H+移向Al电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | MgO的熔点很高,可用于制造耐火材料 | |
| B. | (NH4)2SO4浓溶液能使蛋白质溶液发生盐析,可用于杀菌消毒 | |
| C. | 常温下Al与浓硝酸不反应,可以用铝槽车运输浓硝酸 | |
| D. | 碳具有强还原性,高温下能将二氧化硅还原为硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com