
| A. | 辉石、斜长石及橄榄石均属于硅酸盐矿 | |
| B. | 斜长石的氧化物形式可表示为:K2O•Al2O3•6SiO2 | |
| C. | 橄榄石中铁为+2价 | |
| D. | 月球上有游离态铁是因为月球上铁的活性比地球上铁的活动性弱 |
分析 A.辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石[(Mg,Fe)2SiO4]的成分均属于硅酸盐类;
B.根据硅酸盐的氧化物表示方法来书写;
C.根据元素的化合价规则来判断铁元素的化合价;
D.金属的活动性是金属本身的性质,和金属所在的位置无关;
解答 解:A.辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石[(Mg,Fe)2SiO4]的成分均属于硅酸盐类,均属于硅酸盐矿,故A正确;
B.硅酸盐的氧化物表示方法:先写活泼金属氧化物,然后是不活泼的金属氧化物,再是非金属氧化物二氧化硅,最后是水,所以斜长石的氧化物形式可表示为:K2O•Al2O3•6SiO2,故B正确;
C.化合物中化合价代数和为0,镁元素化合价是+2价,硅元素化合价是+4价,氧元素化合价是-2价,所以铁元素化合价是+2价,故C正确;
D.金属铁的活动性是金属本身的性质,和金属是在月球上还是在地球上无关,只是月球上没有氧气,在月球上存在游离态铁,故D错误;
故选D.
点评 本题考查学生有关硅酸盐的知识,注意硅酸盐的氧化物形式书写方法,注意平时知识的积累是解题的关键,题目难度不大.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑦⑧⑨ | B. | ②④⑥⑦⑧⑨ | C. | ①④⑥⑧ | D. | ①②④⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若管道漏气遇氨会产生白烟 | B. | 该反应利用了氯气的强氧化性 | ||
| C. | 该反应属于复分解反应 | D. | 生成1 mol N2有6 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-lg2 | B. | b-lg2 | C. | a+lg2 | D. | b+lg2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
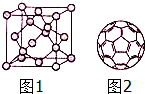 碳及化合物与人类的关系非常密切,对碳单质及其化合物的研究具有重要意义.
碳及化合物与人类的关系非常密切,对碳单质及其化合物的研究具有重要意义.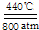 2Na2CO3+C;CO32-的空间构型为平面正三角形(用文字描述).
2Na2CO3+C;CO32-的空间构型为平面正三角形(用文字描述).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
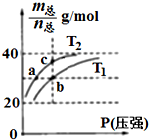 已知(HF)2(g)?2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )
已知(HF)2(g)?2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )| A. | 温度:T1<T2 | |
| B. | 平衡常数:K(a)=K(b)<K(c) | |
| C. | 反应速率:Vb>Va | |
| D. | 当$\frac{m(总)}{n(总)}$=30g/mol时,n(HF):n(HF)2=2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
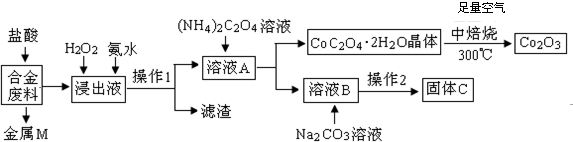
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验.
某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验.| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | BaSO4 | BaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+8-m-n | B. | a+16-m-n | C. | a-8-(m+n) | D. | a-(m+n) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com