
分析 根据物质的量n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$分别进行计算含有氧气分子数、水分子、二氧化碳的物质的量、氢气气体体积及氧原子数.
解答 解:(1)0.1mol O2中含有的氧分子数为:N(O2)=nNA=0.1NA,
故答案为:0.1NA;
(2)1.204×1024个水分子的物质的量为:$\frac{1.204×1{0}^{24}}{6.02×1{0}^{23}mo{l}^{-1}}$=2mol,
故答案为:2mol;
(3)22g CO2的物质的量为:n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,
故答案为:0.5mol;
(4)标准状况下0.5molH2的体积为:22.4L/mol×0.5mol=11.2L,
故答案为:11.2L;
(5)1molH2SO4中含有氧原子的物质的量为:n(O)=1mol×4=4mol,含有的氧原子数为4NA,
故答案为:4NA.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数之间的关系即可解答,试题培养了学生的化学计算能力.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:实验题
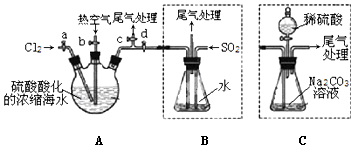
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
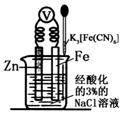
| A. | 该装置为电解池 | |
| B. | 本实验牺牲了金属Fe来保护金属Zn | |
| C. | 若加入K3[Fe(CN)6]溶液后,Fe电极附近不会产生特征蓝色的沉淀 | |
| D. | 远洋货轮上镶嵌的金属Zn长时间没有什么变化,不需要更换 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 一般不用纯碱代替小苏打作食品发酵粉 | |
| C. | 用甲醛溶液浸泡海产品以保鲜 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
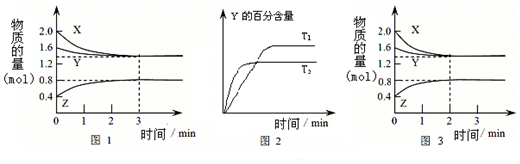
| A. | 容器中发生的反应可表示为:2X(g)+Y(g)?2Z(g) | |
| B. | 0~3 min内,v(X)=0.2 mol•L-1•min-1 | |
| C. | 其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 | |
| D. | 若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
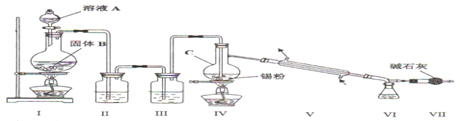
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com