
| A、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |
| B、醋酸与NaHCO3溶液反应:H++HCO3-=CO2↑+H2O |
| C、将少量铜屑放入浓硝酸中的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学反应的同时都伴随着能量变化 |
| B、伴随能量变化的过程都是化学变化 |
| C、在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 |
| D、并不是所有的化学变化都伴随着能量的放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
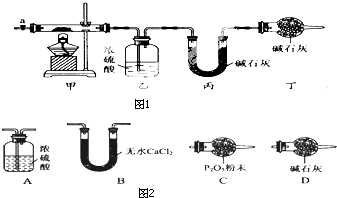 碱式碳酸钴[Cox(OH)y(C03)z]常用作电子材料、磁性材料的添加剂,受热时可分解生喊三种氧化物.为了确定其组成,某化学兴趣小组同学设计了如图1所示的装置进行实验.
碱式碳酸钴[Cox(OH)y(C03)z]常用作电子材料、磁性材料的添加剂,受热时可分解生喊三种氧化物.为了确定其组成,某化学兴趣小组同学设计了如图1所示的装置进行实验.| 乙装置的质量/g | 丙装置的质量/g | |
| 加热前 | 80.00 | 62.00 |
| 加热后 | 80.36 | 62.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 自然界中氮元素有多种存在形式.
自然界中氮元素有多种存在形式.
查看答案和解析>>
科目:高中化学 来源: 题型:
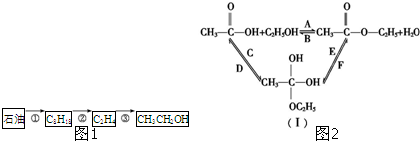
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com